
| 一般情况 | |
|---|---|
 | 品种:马尔济斯犬 |
| 年龄:5岁 | |
| 性别:雌 | |
| 是否绝育:否 | |
| 诊断:胃底腺息肉 | |
01 主诉及病史
慢性间歇性呕吐一年多。该犬5年前曾因MRI发现侧脑室扩张而被诊断为脑积水,并接受了呋塞米(1 mg/kg,q12 h)和奥美拉唑(0.7-1.0 mg/kg,q24 h)口服治疗以减少脑脊液容量。
1年前该犬出现更频繁的全身强直阵挛发作,奥美拉唑剂量增加到10 mg/kg。本次就诊时,癫痫发作的频率有所下降,但呕吐的频率有所增加。
02 检查
嗜睡,身体状况评分正常(3/9),心动过速(>180 bpm),其他生命体征正常。口腔粘膜呈粉红色,毛细血管再充盈时间小于2秒。
触诊未发现腹痛,神经系统检查结果无异常。全血细胞计数和血清电解质浓度均无异常。生化分析显示血尿素氮水平较高(33.7 mg/dL,参考:7-28)。放射线检查无异常。
腹部超声显示胃壁明显增厚,有多叶状增厚皱襞和无回声囊肿。胃壁层无法分辨,胃黏膜呈高回声,无淋巴结病变(下图)。
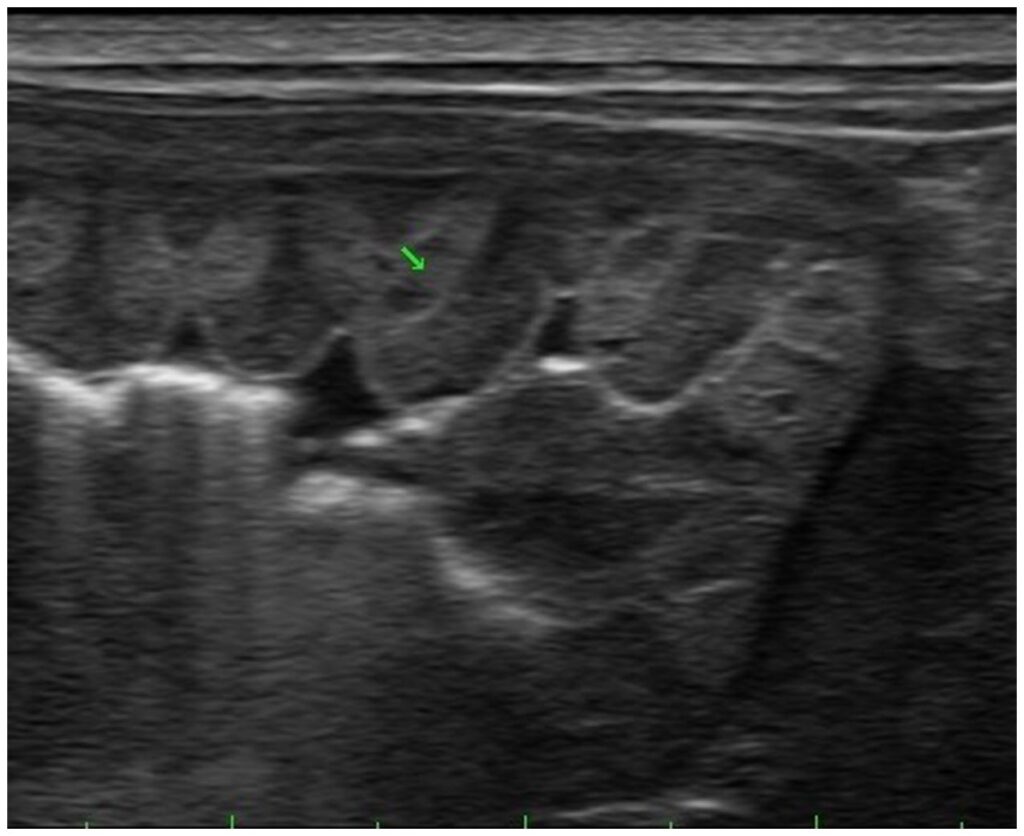
胃镜证实患者存在明显的胃皱襞肥大和息肉样病变(下图)。巨大的胃皱襞横跨大部分胃体和部分胃底。整个胃体都有息肉,没有发现糜烂或溃疡。
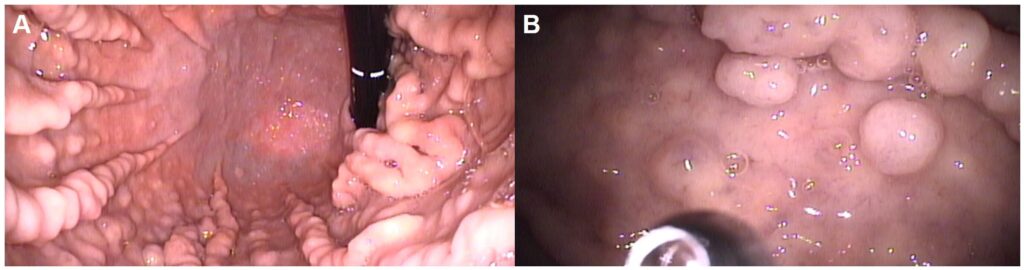
息肉组织学检查显示细胞弥漫性增生,但无窝状增生,胃腺偶有囊性扩张(下图A)。观察到明显的顶叶细胞增生,主细胞数量减少(下图B)。基质中含有多灶性炎症浸润,包括淋巴细胞、浆细胞和固有膜中偶尔出现的嗜酸性粒细胞(下图C)。大多数增生的顶叶细胞呈多形性,胞浆空泡化(下图D)。
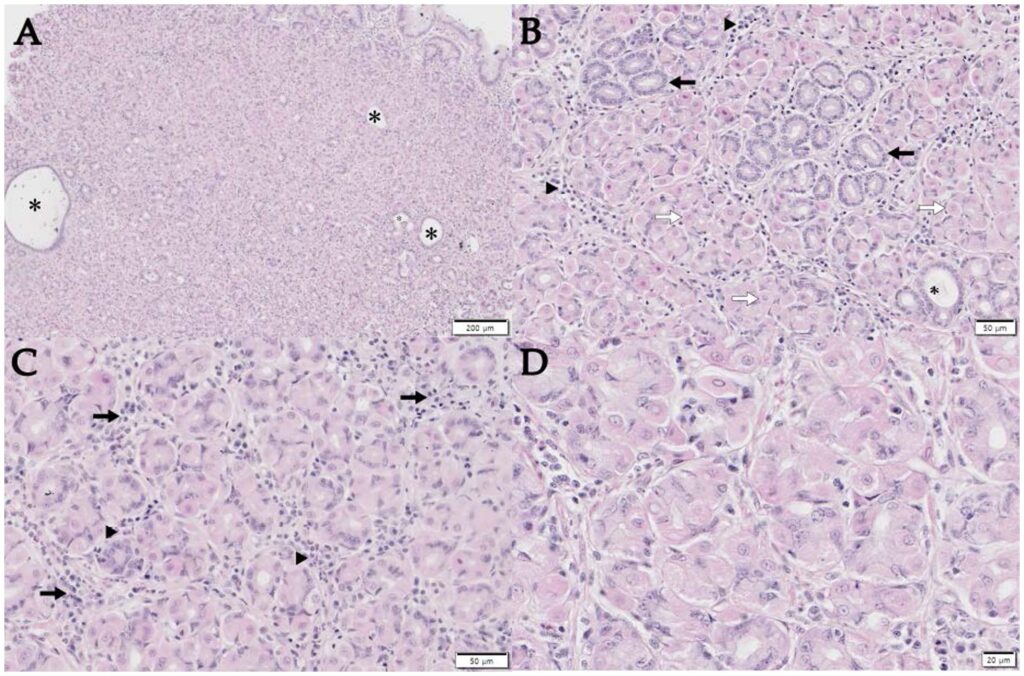
03 治疗及预后
停止服用奥美拉唑,并口服泼尼松龙(0.25 mg/kg,q12 h)。使用碘125测量血清胃泌素浓度,结果显示浓度较高(78.4 ng/L,参考:10-40)。
停用奥美拉唑1个月后,主人报告说呕吐次数减少。
停用奥美拉唑2个月后,呕吐症状消失,胃壁和胃皱襞增厚的情况也有所改善,但仍未完全恢复正常(下图A)。应主人的要求,没有进行进一步的内镜和组织病理学检测。
停用奥美拉唑48个月后,该犬仍然存活,没有呕吐等临床症状。胃部超声检查结果并不明显(下图B),血清胃泌素浓度在正常范围内(21.3 ng/L)。
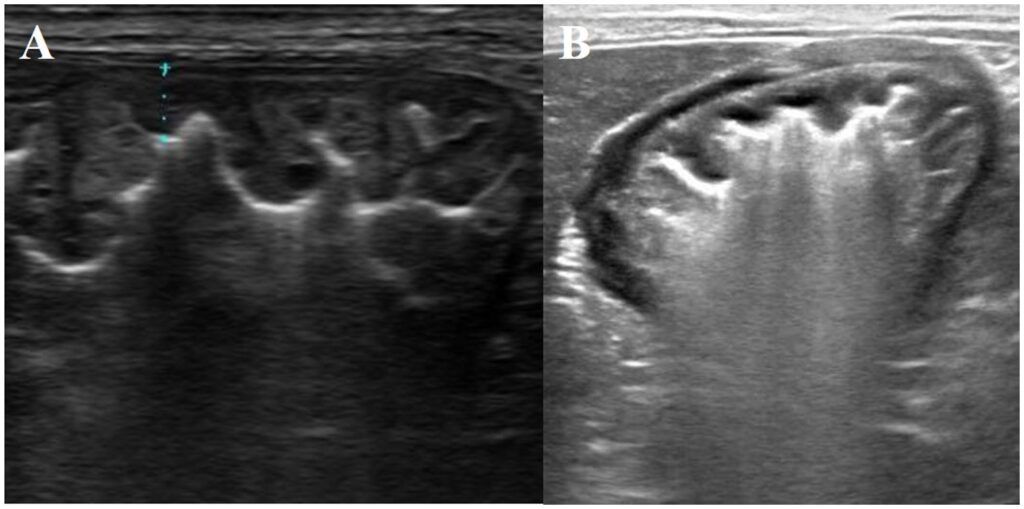
04 讨论
质子泵抑制剂(PPI)是治疗人类和动物多种疾病的常用抑酸剂。这类药物也可用于长期治疗犬脑积水[1]。由于在没有明确适应症的情况下使用PPI可能会产生不良反应,因此人们对不适当或长期使用PPI提高了警惕[2,3]。长期使用PPI的不良反应大多发生在人类身上,而对狗的影响则缺乏证据[3]。
在人类中,长期使用PPI可观察到胃粘膜的组织病理学变化。这些变化在内窥镜检查中表现为胃底腺息肉、增生性息肉、多发性白色扁平隆起病变、鹅卵石样粘膜或黑斑[4]。兽医文献中尚未发现这些胃部变化。
根据以往的兽医研究,由于不良反应的风险增加,在有明确适应症的情况下使用PPI的考虑不足[5],但这些研究并不关注狗长期使用PPI的情况[6-9]。因此,尽管这些药物被广泛使用,但其潜在的不良反应(包括长期使用PPI引起的胃部变化)在兽医学中仍不明确。本病例描述了一例因长期服用奥美拉唑治疗脑积水而出现胃底腺息肉的犬。
口服奥美拉唑可提高犬的胃pH值[14],从而消除胃酸对G细胞分泌的抑制作用,进一步刺激胃泌素的释放[15]。这导致胃顶叶细胞分泌的胃酸更多,就像人类一样[11,13,16],并引起胃顶叶细胞肥大和向腺体管腔突出,导致腺体管腔阻塞和囊肿形成。肥大性胃息肉随着囊肿的增大而形成[13]。
有胃皱襞增厚和息肉的疾病需要根据其发病机制和组织病理学特征进行鉴别诊断。梅内特里埃氏病(Menetrier’s-like disease)是一种出现在胃体和胃底的疾病,其组织学特征是胃窝增生和胃顶萎缩[17,18]。幽门螺杆菌和巨细胞病毒感染与人类和小鼠的梅内特里埃病有关[19,20],但犬的梅内特里埃病是否由PPI诱发尚不清楚。
肥大性分泌过多性胃病的特征是严重的窝状增生和顶叶增生。然而,本患者表现为顶叶增生而无窝状增生,尽管它们的临床和内镜检查结果相似,但这些组织病理学上的差异有助于区分和诊断它们。
有些疾病因其特征相似而无法通过内镜或组织病理学加以区分。佐林-艾利森综合征(Zollinger-Ellison syndrome,ZES)不仅在内镜下表现为胃皱襞增厚,而且在组织病理学上表现为顶叶增生而无窝状增生[21]。
ZES是由十二指肠或胰腺胃泌素瘤引起的,而胃泌素瘤起源于G细胞。胃泌素瘤大量释放的胃泌素可激活ECL细胞,导致组胺的合成和分泌。胃泌素和组胺刺激胃顶叶细胞分泌盐酸和来自D细胞的体泌素,从而产生负反馈,胃泌素瘤破坏了这种负反馈,导致ECL和顶叶细胞增生[22]。
此外,大多数ZES患者会因严重的高胃泌素血症而出现胃溃疡[23]。本患者虽然血清胃泌素浓度高于参考值,但却没有胃溃疡和肿瘤。此外,PPI可以有效治疗犬ZES[24]。腹部超声检查没有胃泌素瘤的证据,患者存活了4年,没有任何ZES的临床症状。
本文报告的这只狗每24小时口服0.7-1.0 mg/kg的奥美拉唑,已经持续了4年多。关于犬长期服用PPI的不良反应的描述很少,但腹泻是犬最常见的不良反应[25]。兽医文献还指出,长期服用PPI有可能导致高胃泌素血症,从而诱发胃肿瘤[3,12]。
本文报告的这只狗的血清胃泌素浓度较高,但由于分析是在不同的实验室进行的,因此无法与之前报告的健康狗的血清胃泌素浓度[12]进行直接比较。高胃泌素血症是奥美拉唑抑制胃酸分泌的次要原因,可能是本病例胃底腺息肉的原因,人类也是如此[13]。
停止使用PPI后,胃部病变可能会逆转[16],本患者就出现了这种情况。胃部病变的改善可能是由于停止使用奥美拉唑后血清胃泌素浓度恢复正常所致。然而,有必要进行进一步研究,以证实奥美拉唑引起的高胃泌素血症与狗的肥厚性胃病有关。
奥美拉唑治疗的持续时间和剂量可能是诱发胃底腺息肉的重要因素。在人类医学中,与长期服用PPI相关的胃部不良反应一般发生在超过1年之后[10]。在一项研究中,每天给狗服用 0.7 mg/kg的奥美拉唑,持续时间超过1年,却没有发现任何胃部变化,只有在每天服用奥美拉唑剂量超过5.5 mg/kg的狗中才发现了与本病例类似的胃底皱襞肥大[26]。这表明奥美拉唑只有在长期(>1年)、高剂量(>5.5 毫克/千克/天)给药的情况下才会诱发犬胃底腺息肉。
本文描述的这只狗曾连续4年每24小时口服0.7-1.0 mg/kg奥美拉唑,后来剂量逐渐增加到每24小时口服10 mg/kg。因此,长期服用大剂量奥美拉唑的狗可能会出现胃底腺息肉。有必要进行进一步研究,以确定奥美拉唑可能诱发胃底腺息肉的用药时间和剂量。
参考文献
[1] Thomas WB. Hydrocephalus in dogs and cats. Vet Clin North Am Small Anim Pract. (2010) 40:143–59.
[2] Nehra AK, Alexander JA, Loftus CG, Nehra V. Proton pump inhibitors: review of emerging concerns. Mayo Clin Proc. (2018) 93:240–6.
[3] Marks SL, Kook PH, Papich MG, Tolbert MK, Willard MD. ACVIM consensus statement: support for rational administration of gastrointestinal protectants to dogs and cats. J Vet Intern Med. (2018) 32:1823–40.
[4] Kim GH. Proton pump inhibitor-related gastric mucosal changes. Gut Liver. (2021) 15:646–52.
[5] Duxbury S, Sorah E, Tolbert MK. Evaluation of proton pump inhibitor administration in hospitalized dogs in a tertiary referral hospital. J Vet Intern Med. (2022) 36:1622–7.
[6] Eichstadt LR, Moore GE, Childress MO. Risk factors for treatment-related adverse events in cancer-bearing dogs receiving piroxicam. Vet Comp Oncol. (2017) 15:1346–53.
[7] Jones SM, Gaier A, Enomoto H, Ishii P, Pilla R, Price J, et al.. The effect of combined carprofen and omeprazole administration on gastrointestinal permeability and inflammation in dogs. J Vet Intern Med. (2020) 34:1886–93.
[8] McCormack R, Olley L, Glanemann B, Swann JW. Prospective observational study of the use of omeprazole and maropitant citrate in veterinary specialist care. Sci Rep. (2020) 10:15727.
[9] Shaevitz MH, Moore GE, Fulkerson CM. A prospective, randomized, placebo-controlled, double-blinded clinical trial comparing the incidence and severity of gastrointestinal adverse events in dogs with cancer treated with piroxicam alone or in combination with omeprazole or famotidine. J Am Vet Med Assoc. (2021) 259:385–91.
[10] Jalving M, Koornstra JJ, Wesseling J, Boezen HM, De Jong S, Kleibeuker JH. Increased risk of fundic gland polyps during long-term proton pump inhibitor therapy. Aliment Pharmacol Ther. (2006) 24:1341–8.
[11] Zelter A, Fernández JL, Bilder C, Rodríguez P, Wonaga A, Dorado F, et al.. Fundic gland polyps and association with proton pump inhibitor intake: a prospective study in 1,780 endoscopies. Dig Dis Sci. (2011) 56:1743–8.
[12] Parente NL, Bari Olivier N, Refsal KR, Johnson CA. Serum concentrations of gastrin after famotidine and omeprazole administration to dogs. J Vet Intern Med. (2014) 28:1465–70.
[13] Cats A, Edschenk B, Bloemena E, Roosendaal R, Lindeman J, Biemond I, et al.. Parietal cell protrusions and fundic gland cysts during omeprazole maintenance treatment. Hum Pathol. (2000) 31:684–90.
[14] Tolbert K, Bissett S, King A, Davidson G, Papich M, Peters E, et al.. Efficacy of oral famotidine and 2 omeprazole formulations for the control of intragastric pH in dogs. J Vet Intern Med. (2011) 25:47–54.
[15] Herdt TH. Secretions of the gastrointestinal tract In: Klein BG, editor. Cunningham’s textbook of veterinary physiology. 6th ed: St.Louis, Missouri, USA: Elsevier; (2020). 307–15.
[16] Parks T, Ragland KL, Steiner MA, Subramony C, Bishop P, Nowicki M. Ménétrier mimicker complicating ulcerative colitis: proton-pump inhibitor-induced hyperplastic polyps. J Pediatr. (2015) 167:776.e1.
[17] Munday JS, Aberdein D, Cullen GD, French AF. Ménétrier disease and gastric adenocarcinoma in 3 cairn terrier littermates. Vet Pathol. (2012) 49:1028–31.
[18] Vaughn DP, Syrcle J, Cooley J. Canine giant hypertrophic gastritis treated successfully with partial gastrectomy. J Am Anim Hosp Assoc. (2014) 50:62–6.
[19] Badov D, Lambert JR, Finlay M, Balazs ND. Helicobacter pylori as a pathogenic factor in Ménétrier’s disease. Am J Gastroenterol. (1998) 93:1976–9.
[20] Huh WJ, Coffey RJ, Washington MK. Ménétrier’s disease: its mimickers and pathogenesis. J Pathol Transl Med. (2016) 50:10–6.
[21] Roy PK, Venzon DJ, Shojamanesh H, Abou-Saif A, Peghini P, Doppman JL, et al.. Zollinger-Ellison syndrome. Clinical presentation in 261 patients. Medicine (Baltimore). (2000) 79:379–411.
[22] Burkitt MD, Varro A, Pritchard DM. Importance of gastrin in the pathogenesis and treatment of gastric tumors. World J Gastroenterol. (2009) 15:1–16.
[23] Deveney CW, Deveney KE. Zollinger-Ellison syndrome (gastrinoma). Current diagnosis and treatment. Surg Clin North Am. (1987) 67:411–22.
[24] Brooks D, Watson GL. Omeprazole in a dog with gastrinoma. J Vet Intern Med. (1997) 11:379–81.
[25] Davis MS, Willard MD, Nelson SL, McCullough S, Mandsager RE, Roberts J, et al.. Efficacy of omeprazole for the prevention of exercise-induced gastritis in racing Alaskan sled dogs. J Vet Intern Med. (2003) 17:163–6.
[26] The European Agency for the Evaluation of Medicinal Products Veterinary Medicines and Inspections . Committee for veterinary medicinal products Omeprazole; (2002).