| 病例1 | |
|---|---|
 | 品种:约克夏梗 |
| 年龄:3个月 | |
| 性别:雄 | |
| 是否绝育:否 | |
| 诊断:颗粒性小脑皮质变性 | |
01 主诉及病史
从8周大开始出现四肢进行性小脑共济失调和意向性震颤,眼球运动正常。该犬的4个同窝幼仔均正常。
02 检查
神经系统检查发现,该犬有宽大的站立姿势和小脑共济失调症状,特征是四肢发育不全、头颈部意向性震颤和双侧没有威胁反应,但视力正常。神经解剖定位在小脑。
血生化和全血细胞计数均正常。弓形虫和犬新孢子虫血清学检测呈阴性。
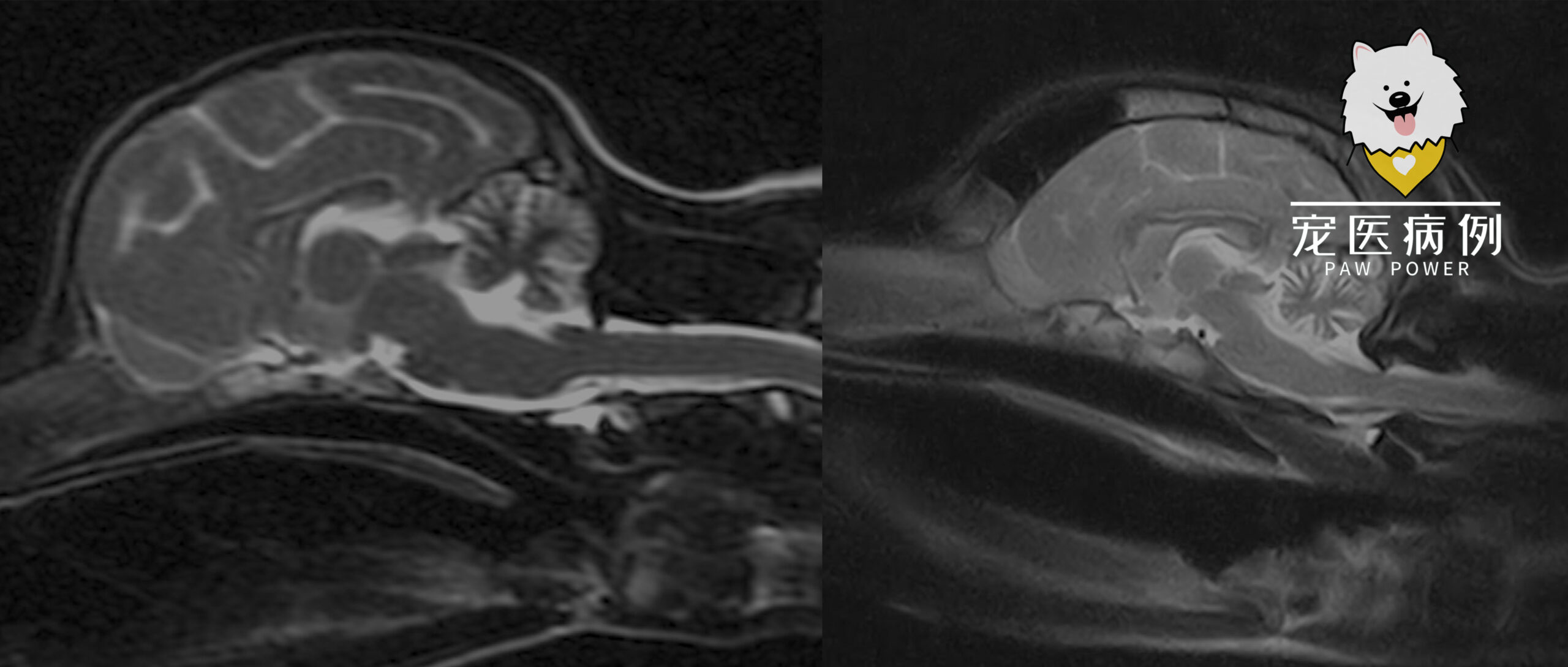
全麻下对头部进行了MRI,结果显示小脑蚓部和半球的小叶明显弥漫性变小,小脑裂明显增宽,T1加权、T2加权和液体衰减反转恢复序列显示与脑脊液等密度的液体(下图)。未观察到椎间孔疝。脑干与小脑的面积比为101%(正常应小于96%),表明小脑体积缩小。
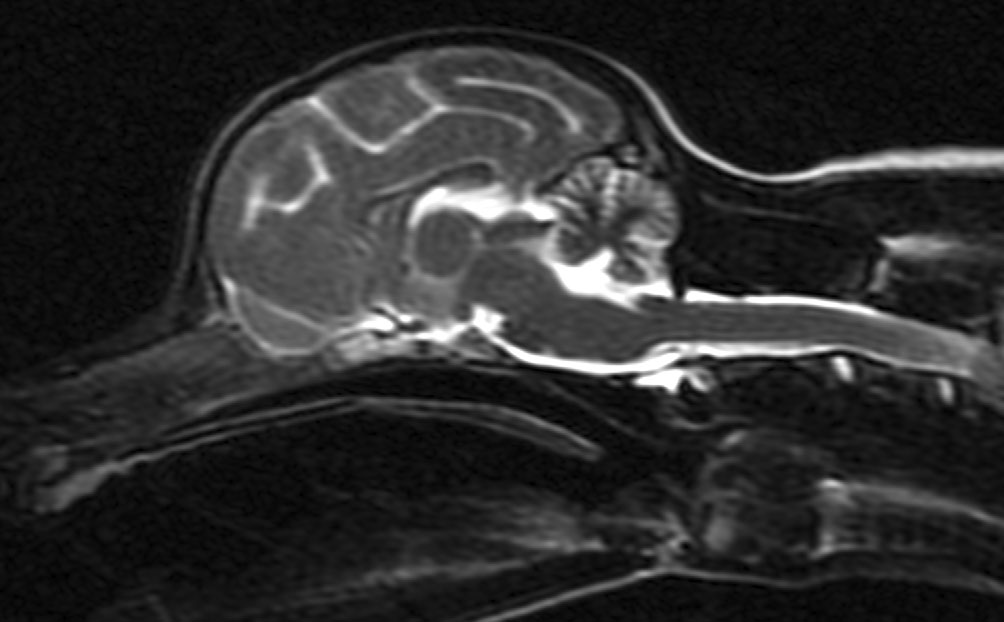
从小脑髓质贮水池采集了脑脊液,包括总核细胞数和蛋白质浓度在内的结果均正常。对脑脊液进行的犬新孢子虫和弓形虫PCR检测呈阴性。
03 预后
由于在初次发病2周后临床症状逐渐恶化,导致无法在没有帮助的情况下行走和进食,主人选择了安乐死,并同意进行尸检。
04 尸检
解剖发现小脑蚓部和半球的小叶明显缩小,切片后皮质明显变薄。显微镜下,小脑叶明显变平。观察到颗粒细胞层弥漫性变薄和细胞减少,颗粒细胞神经元明显缺失,导致该层几乎完全缺失,并伴有中度神经胶质增生(下图)。
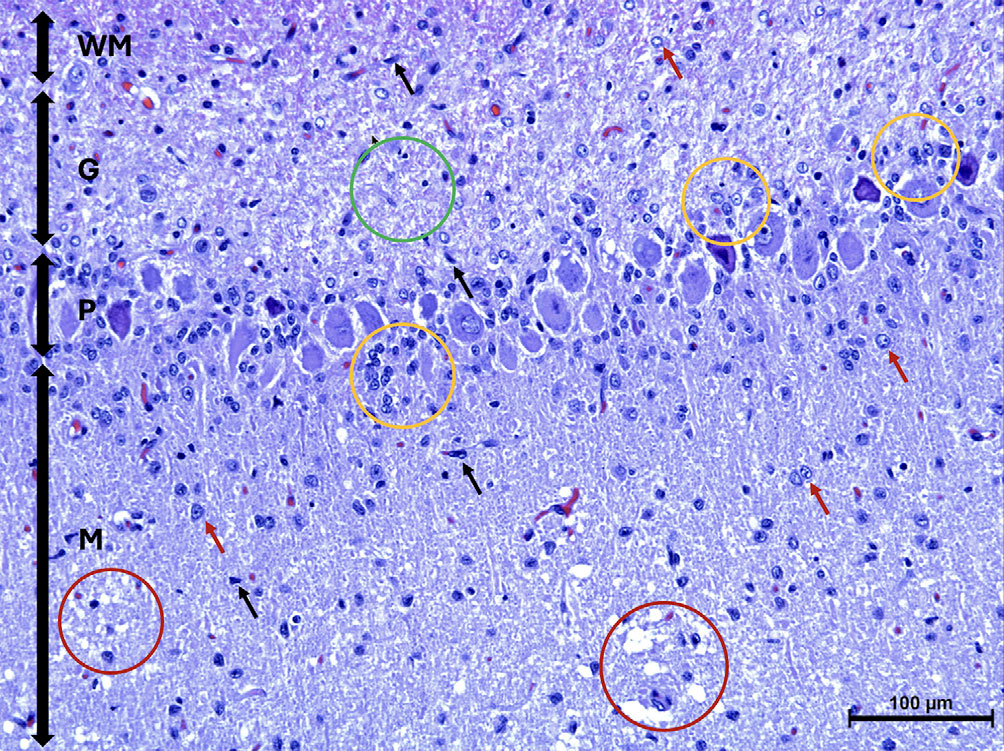
浦肯野神经元细胞体增大,苍白的颗粒状物质堆积,导致核周围的尼氏颗粒移位和堆积。同样的物质在分子层积聚,并伴有中度胶质增生,主要由星形胶质细胞和一些Bergmann胶质细胞组成。在分子层神经髓质中观察到多个海绵状病灶。浦肯野神经元也明显出现大小不等的元内空泡堆积。小脑、一般躯体传出眼球运动和红核的一些神经元颜色苍白,并受到弥漫性胶质病变的影响。大脑的其余部分组织学正常。根据这些发现,最终确诊为颗粒性小脑皮质变性。
| 病例2 | |
|---|---|
 | 品种:拉戈托罗马阁挪露犬 |
| 年龄:7个月 | |
| 性别:雄 | |
| 是否绝育:否 | |
| 诊断:颗粒性小脑皮质变性 | |
05 主诉及病史
4个月前出现累及四肢的进行性小脑共济失调以及头颈部的意向性震颤,眼球运动正常。该犬的5个同窝幼仔均正常。
06 检查
神经系统检查显示,该幼犬有宽大的站立姿势和小脑共济失调症状,特征是四肢发育不全、头颈部意向性震颤和双侧没有威胁反应,但视力正常。神经解剖定位在小脑。
血生化和全血细胞计数均正常。自噬相关的ATG4D基因突变与拉戈托罗马阁挪露犬的细胞内空泡贮积症有关,通过基因检测未发现基因异常,排除了该病的可能性。弓形虫和犬新孢子虫血清学检测呈阴性。
全麻下对头部进行了MRI,结果显示小脑蚓部和半球的小叶明显弥漫性变小,小脑裂明显增宽,T1加权、T2加权和流体衰减反转恢复序列显示与脑脊液等密度的流体(下图)。未观察到造影剂增强或椎间孔疝。脑干与小脑面积比为132%(正常应小于96%),表明小脑体积缩小。
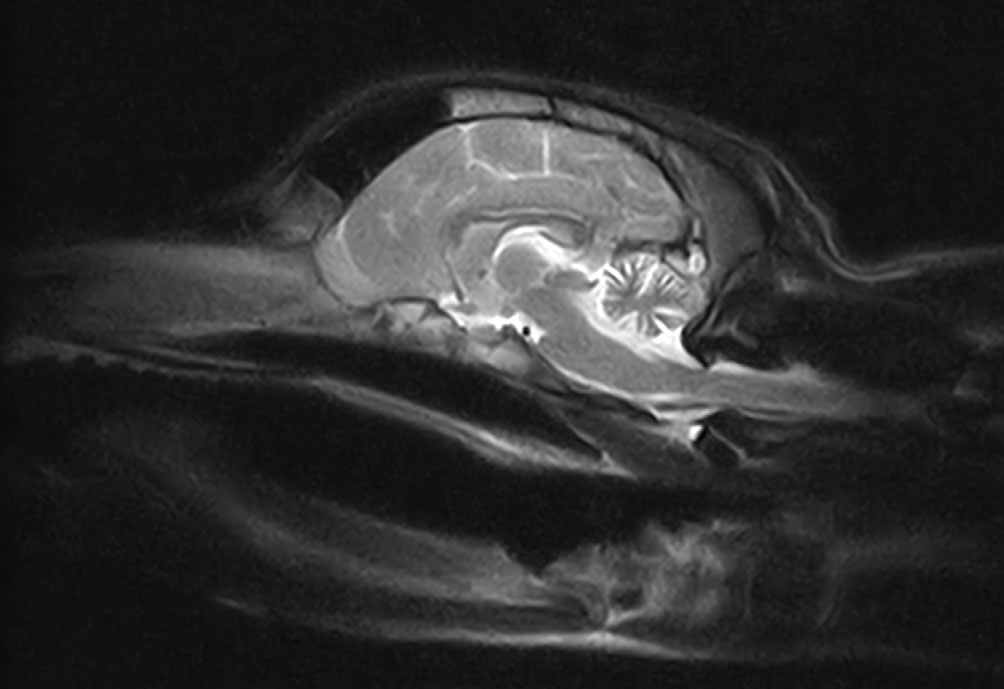
从小脑髓室采集了脑脊液,分析结果(包括总核细胞数和蛋白质浓度)均正常。对脑脊液进行的犬瘟热病毒、巴尔通体、隐球菌、布氏杆菌、犬新孢子虫和弓形虫PCR检测结果均为阴性。
07 预后
在接下来的9个月中,该犬的临床症状一直保持稳定,直到症状迅速恶化,导致该犬无法行走。主人考虑到该犬的生活质量受到影响,决定对其实施安乐死,并同意进行尸检。
08 尸检
解剖发现小脑蚓部和半球的小叶均弥漫性缩小,切片后皮质明显变薄。显微镜下,小脑叶明显变平。观察到颗粒细胞层明显弥漫性变薄和功能减退,颗粒细胞明显丢失,导致该层几乎完全缺失,神经膜明显空泡化(下图)。少数残存的颗粒细胞肿胀、空泡化或萎缩,细胞核萎缩。该层弥漫存在以星形胶质细胞为主的神经胶质细胞。
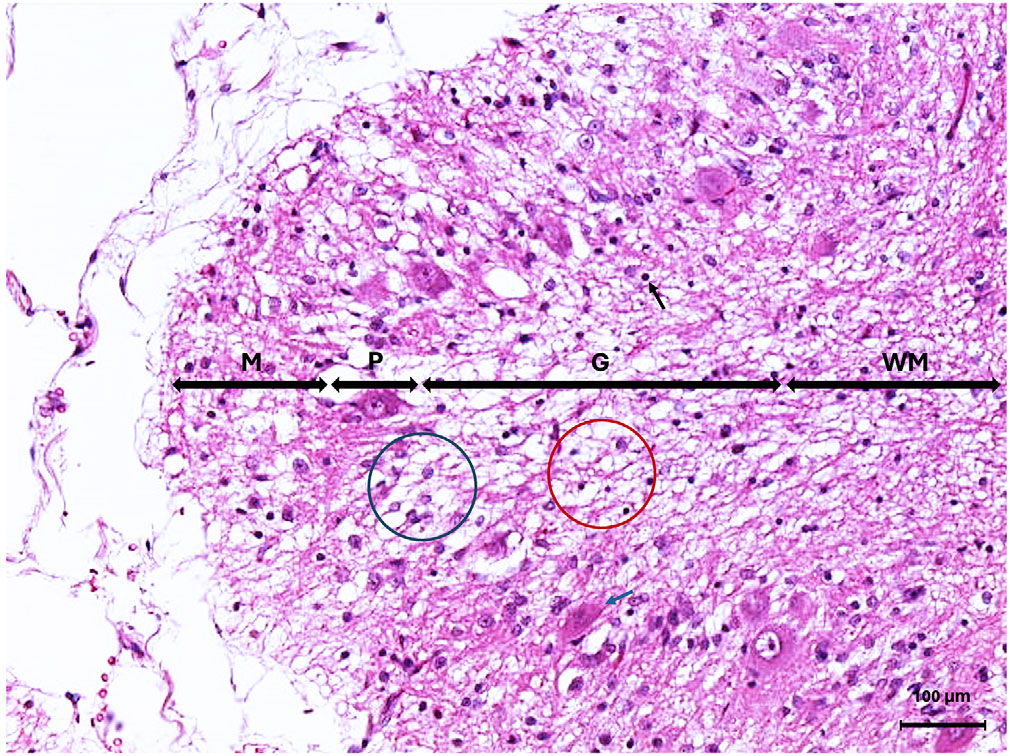
分子层的厚度也轻度减少,但其他方面并无异常。浦肯野细胞层除罕见的浦肯野细胞丢失外,似乎未受影响。在多处,少数散在的浦肯野细胞表现出萎缩、成角、嗜酸性细胞质过多和细胞核萎缩,或极少数细胞核肿胀并伴有中心色素溶解。在间脑白质中弥漫性地观察到胶质细胞中度增加。大脑其余部分组织学正常。根据这些发现,最终确诊为颗粒性小脑皮质变性。
09 讨论
小脑皮质变性(CCD)是一组以小脑皮质的产后变性为特征的疾病[1]。小脑皮质变性根据主要细胞靶点(小脑皮质的浦肯野神经元或颗粒细胞神经元)进行分类[1]。
在大多数患有CCD的犬中,浦肯野神经元是主要靶点,颗粒细胞神经元继发逆行变性[1]。也有报道称,有零星的颗粒细胞神经元选择性缺失,而浦肯野神经元则相对缺失,这被称为颗粒变性[2-11]。其中包括边境牧羊犬、拉布拉多猎犬、巴伐利亚山地犬和柯顿杜勒犬等犬种一窝中多只幼犬受影响的报道,以及澳大利亚凯尔皮犬、意大利猎犬和拉格托-罗马涅罗犬等犬种单个病例的报道[2-11]。
本病例报道报告了第一例和第二例经组织病理学证实的约克夏梗和拉戈托罗马阁挪露犬颗粒性CCD病例。
颗粒性CCD是一种相对少见的CCD,其确切病因仍有待阐明,可能是多因素造成的[1,5,9-11]。有报道称犬疱疹病毒可导致颗粒细胞耗竭,伴有浦肯野神经元缺失、单核细胞浸润灶和畸形[13]。
猫细小病毒宫内感染或围产期感染可导致猫颗粒细胞层发育不良,犬细小病毒在犬小脑发育不良病例中也被检测到,但在CCD病例中没有发现[14,15]。另外,鉴于颗粒细胞层存在明显的弥漫性T细胞浸润,因此怀疑CCD是免疫介导的[5]。
在上述2个病例中,组织病理学检查结果与感染或免疫介导的病因不一致,因为没有炎性细胞浸润或血管周围袖套。此外,传染病检测结果为阴性。鉴于大多数颗粒性CCD病例缺乏免疫介导或感染性组织病理学改变,即使个别幼犬患病,也要怀疑其遗传基础[2-4,6-12]。
同样,在上述2例病例中,由于排除了感染性和炎症性病因,而且临床症状在出生后几周内出现,并呈进行性恶化,因此不太可能是肿瘤、外伤和血管性病因,因此怀疑很可能是遗传引起的退行性病变。不过,也不能完全排除代谢性或中毒性病因。如果颗粒变性的遗传基础被确定,常染色体隐性遗传模式可以解释这两个病例中出现的单个患病幼犬[6]。
病例1在幼年时出现临床症状,病情发展缓慢。病例2在幼年时开始出现临床症状,最初进展缓慢,9个月后病情趋于稳定,然后迅速恶化。病例2的临床症状发病年龄与唯一一例在拉戈托罗马阁挪露犬中报告的颗粒性CCD病例相似,但临床症状的发展与之前报告的病例不同,后者的临床症状发展迅速[8]。
小脑皮质变性主要累及浦肯野神经元,神经元异位症累及大脑、脑桥和小脑,也曾作为单个病例在拉戈托罗马阁挪露犬中报道过,目前仍不确定这些病例是否代表一种涉及神经元迁移或神经元发育和存活的单一疾病谱,或两者兼而有之[8,27]。
由于CCD是一种退行性疾病,没有已知的治疗方法,因此临床症状会不断发展,直至生活质量受到影响,此时通常会实施安乐死[1]。据报道,所有患有颗粒性CCD的犬都是在出现临床症状4周到6个月后因生活质量下降而被实施安乐死[2-11]。
总之,本病例报道报告了第一例和第二例经组织病理学确诊的约克夏梗和拉戈托罗马阁挪露犬颗粒性CCD病例。因此,对于约克夏梗和拉戈托罗马阁挪露犬,如果它们在出生后出现小脑功能障碍的进行性临床症状,则应将颗粒性CCD作为鉴别诊断的一个因素。要确定这些犬种颗粒性CCD的病因,还需要进行更多的研究。
文献来源:Mignan T, Pumarola M, Platt S, James M, Pereira M, Morey-Matamalas A, Recio A. Granuloprival cerebellar cortical degeneration in a Yorkshire Terrier and Lagotto Romagnolo dog. J Vet Intern Med. 2024 Apr 25.
参考文献
1. Urkasemsin G, Olby NJ. Canine hereditary ataxia. Vet Clin North Am. Small Anim Pract. 2014; 44(6): 1075-1089.
2. Perille AL, Baer K, Joseph RJ, Carrillo JM, Averill DR. Postnatal cerebellar cortical degeneration in Labrador Retriever puppies. Canadian Vet J. 1991; 32: 619-621.
3. Tatalick LM, Marks SL, Baszler TV. Cerebellar abiotrophy characterized by granular cell loss in a Brittany. Vet Pathol. 1993; 30: 385-388.
4. Bildfell RJ, Mitchell SK, de Lahunta A. Cerebellar cortical degeneration in a Labrador Retriever. Canadian Vet J. 1995; 36: 570-572.
5. Tipold A, Fatzer R, Jaggy A, Moore P, Vandevelde M. Presumed immune-mediated cerebellar granuloprival degeneration in the Coton de Tuléar breed. J Neuroimmunol. 2000; 110: 130-133.
6. Sandy JR, Slocombe RF, Mitten RW, Jedwab D. Cerebellar abiotrophy in a family of Border Collie dogs. Vet Pathol. 2002; 39: 736-738.
7. Cantile C, Salvadori C, Modenato M, Arispici M, Fatzer R. Cerebellar granuloprival degeneration in an Italian Hound. J Vet Med. A, Physiol, Pathol, Clin Med. 2002; 49(20): 523-525.
8. Jokinen TS, Rusbridge C, Steffen F, et al. Cerebellar cortical abiotrophy in Lagotto Romagnolo dogs. J Small Anim Pract. 2007; 48: 470-473.
9. Flegel T, Matiasek K, Henke D, Grevel V. Cerebellar cortical degeneration with selective granule cell loss in Bavarian Mountain dogs. J Small Anim Pract. 2007; 48: 462-465.
10. Huska J, Gaitero L, Snyman HN, Foster RA, Pumarola M, Rodenas S. Cerebellar granuloprival degeneration in an Australian Kelpie and a Labrador Retriever dog. Canadian Vet J. 2013; 54: 55-60.
11. López Betran M, Mascort J, Pumarola M. Cerebellar granuloprival and trans-synaptic degeneration in a Chihuahua. Vet Rec Case Reports. 2020; 8(1):e000873.
12. Thames RA, Robertson ID, Flegel T, et al. Development of a morphometric magnetic resonance image parameter suitable for distinguishing between normal dogs and dogs with cerebellar atrophy. Vet Radiol Ultrasound. 2010; 51: 246-253.
13. Percy DH, Carmichael LE, Albert DM, King JM, Jonas AM. Lesions in puppies surviving infection with Canine Herpesvirus. Vet Pathol. 1971; 8: 37-53.
14. Vandervelde M, Higgins RJ, Overmann A. Veterinary Neuropathology: Essentials of Theory and Practice. 1st ed. Ames, IA: Wiley-Blackwell; 2012.
15. Schatzberg SJ, Haley NJ, Barr SC, et al. Polymerase chain reaction (PCR) amplification of parvoviral DNA from the brains of dogs and cats with cerebellar hypoplasia. J Vet Intern Med. 2003; 17: 538-544.
16. Huang M, Verbeek DS. Why do so many genetic insults lead to Purkinje cell degeneration and spinocerebellar ataxia? Neurosci Lett. 2019; 688: 49-57.
17. Norman RM. Primary degeneration of the granular layer of the cerebellum: an unusual form of familial cerebellar atrophy occurring in early life. Brain. 1940; 63(4): 365-379.
18. Goulon M, Escourolle R, Barois A, Grosbuis S. Norman type congenital atrophy of the granular layer. Observation of 2 sisters; neuro-pathological examination of a case. Rev Neurol. 1968; 118(1): 87-88.
19. Montgomery DL, Storts RW. Hereditary striatonigral and cerebello-olivary degeneration of the Kerry Blue Terier. II. Ultrastructural lesions in the caudate nucleus and cerebellar cortex. J Neuropathol Exp Neurol. 1984; 43(3): 263-275.
20. Smeyne RJ, Goldowitz D. Development and death of externalgranular layer cells in the weaver mousse cerebellum: a quantitative study. J Neurosci. 1989; 9: 1608-1620.
21. Dahmane N, Ruiz I, Altaba A. Sonic hedgehog regulates the growth and patterning of the cerebellum. Development. 1999; 126(14): 3089-3100.
22. Ming JE, Elkan M, Tang K, Golden JA. Type I bone morphogenetic protein receptors are expressed on cerebellar granular neurons and a constitutively active form of the type IA receptor induces cerebellar abnormalities. Neuroscience. 2002; 114(4): 849-857.
23. Lihua Q, Wine-Lee L, Ahn KJ, et al. Genetic analyses demonstrate that bone morphogenetic protein signaling is required for embryonic cerebellar development. J Neurosci. 2006; 26(7): 1896-1905.
24. Letts VA. Stargazer – a mouse to seize! Epilepsy Curr. 2005; 5(5): 161-165.
25. De Lahunta A, Glass E, Kent M. De Lahunta’s Veterinary Neuroanatomy and Clinical Neurology. 5th ed. Philadelphia, PA: Elsevier; 2020.
26. Kent M, Glass E, de Lahunta A. Cerebellar cortical abiotrophy in a Beagle. J Small Anim Pract. 2000; 41: 321-323.
27. Rusbridge C, Wilkins P. Neuronal heterotopia in a Lagotto Romagnolo dog (Abstract). Neuropathol Appl Neurobiol. 2002; 28: 148-170.