
| 一般情况 | |
|---|---|
 | 品种:普德尔指示犬 |
| 年龄:17个月 | |
| 性别:雌 | |
| 是否绝育:否 | |
| 诊断:异位骨化 | |
01 主诉及病史
因间歇性(持续数月)左前肢跛行就诊,没有明显的疼痛症状。
患者没有外伤史,其父母或同窝兄弟也没有类似症状。之前曾出现过左肩水肿和脓肿,需要反复引流、冲洗和抗菌治疗。
02 检查
体重25千克。体格检查发现左侧肩胛前肿胀,触诊敏感。
神经系统检查发现,左前肢单瘫,跛行程度为2/5级,屈肌反射减弱,患肢出现姿势反应,表明下运动神经元病变。神经解剖定位于左侧臂丛或腹侧角灰质病变,病变位于第六颈椎(C6)和第二胸椎(T2)脊髓节段之间。
全血细胞计数和血生化的所有参数都在正常范围内。
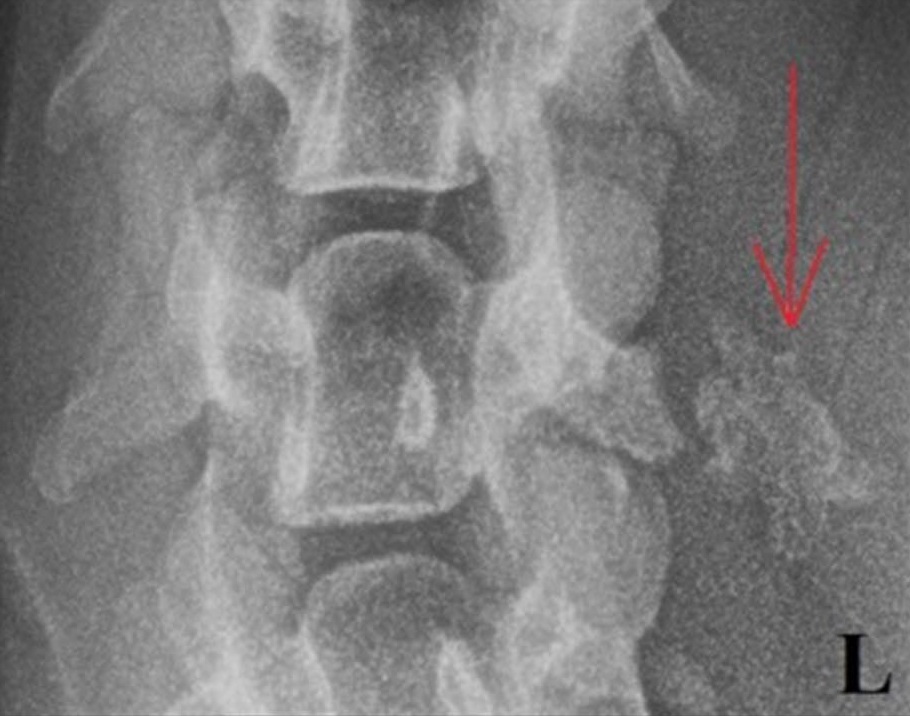
左侧C1-T2脊柱和椎旁组织的常规X光片显示,第五颈椎左侧横突附近有一个边缘不规则的角状钙化(下图)。该横突变钝且不规则,与软组织钙化区域呈棋盘格状。在钙化物周围发现了明显的软组织肿胀。
全麻下MRI显示,在C5椎体左侧的软组织中发现了一个角状结构(10×11×16 mm)。在T2W、T1W和GE T2*图像上,该结构有一个信号空白的薄边缘,看起来像骨皮质,其核心与骨髓等密度。这种钙化结构类似骨的外观,但位于肌肉内。周围肌肉本身是异质的,皮下组织有大量积液,面积达10×2.7 cm——囊性病变的大部分内容呈T1W低密度和T2W高密度;但核心呈T2W/T2*低密度。钙化结构周围的肌肉有一些对比度增强(下图)。
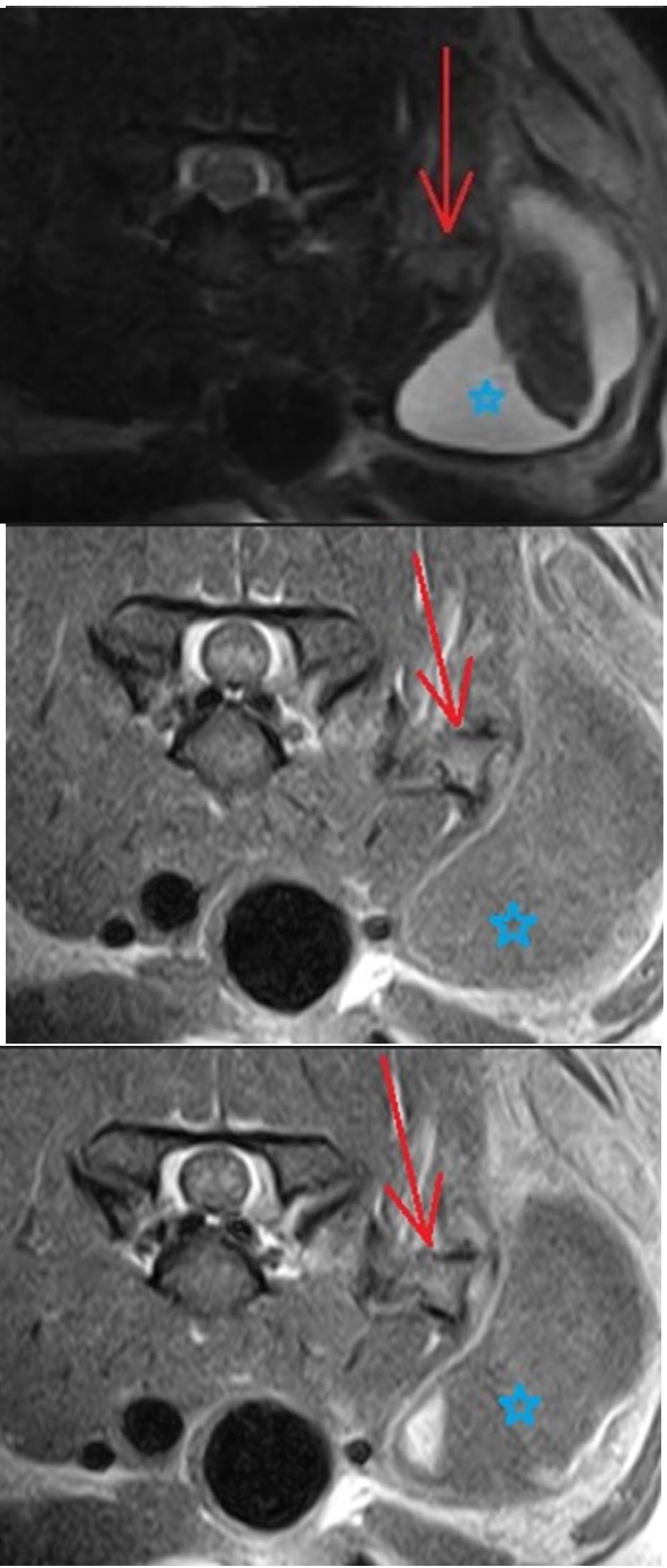
由于出现了”骨”,钙化结构被认为符合异位骨化。囊性病变被认为是带有出血性成分、血肿或潜在脓肿的复杂囊肿/肉瘤。
03 手术
取右侧卧位,前肢向尾部捆绑。在肿块上切开皮肤,牵开胸大肌和胸枕肌。首先剥离骨性肿块上的坚硬包囊。排出液体,露出骨性结构。病变部位的液体和组织样本被送去进行需氧和厌氧培养,结果均为阴性。
病灶附着在颈阔肌上,与C5椎体左侧横突有松散的纤维连接。左侧C6脊神经嵌入骨性肿块中。对肿块进行了解剖,使其脱离纤维附着物,并将其整体移除。
从骨性肿块中仔细、轻柔地剥离和清除被卡住的脊神经。缝合手术部位的组织,并常规缝合伤口。切除的组织送病理学检查,该组织大小为12×18×12 mm,呈部分包裹状,表面不规则,颜色为白色至浅棕色。切口坚硬,有沙砾感(下图)。
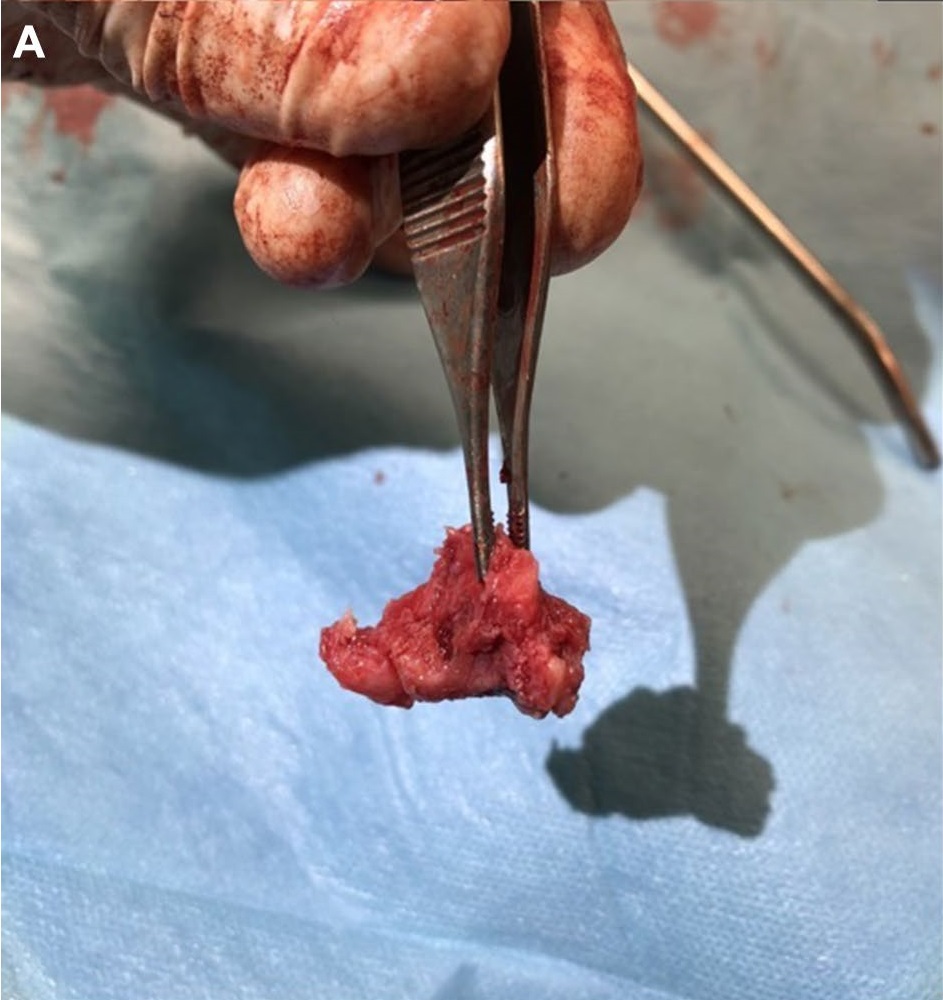
显微镜下表现为由完全分化的编织骨逐渐变为更成熟的片状骨形成的环绕性良好的部分包裹性病灶。骨刺上覆盖着一层细胞过度增生的成骨细胞内膜,其中夹杂着一些破骨细胞。骨膜内层显示出中央造血活跃的红骨髓。
囊由厚厚的平行走向、细胞性差的纤维胶原组织束组成,与片状骨直接接触。沿着包膜,有明显的血管增生,既有动脉也有静脉,偶尔有充满无定形、轻微嗜酸性物质的海绵状空隙,以及数量不等的类似血管肉瘤的管腔内红细胞。血管壁出现中度增厚,平滑肌细胞突出。在一个切片中观察到寡病灶变性软骨形成。囊外的骨骼肌呈轻度至中度萎缩,没有炎症浸润的迹象。形态学诊断为肌肉内成熟的异位骨化伴血管瘤(下图)。
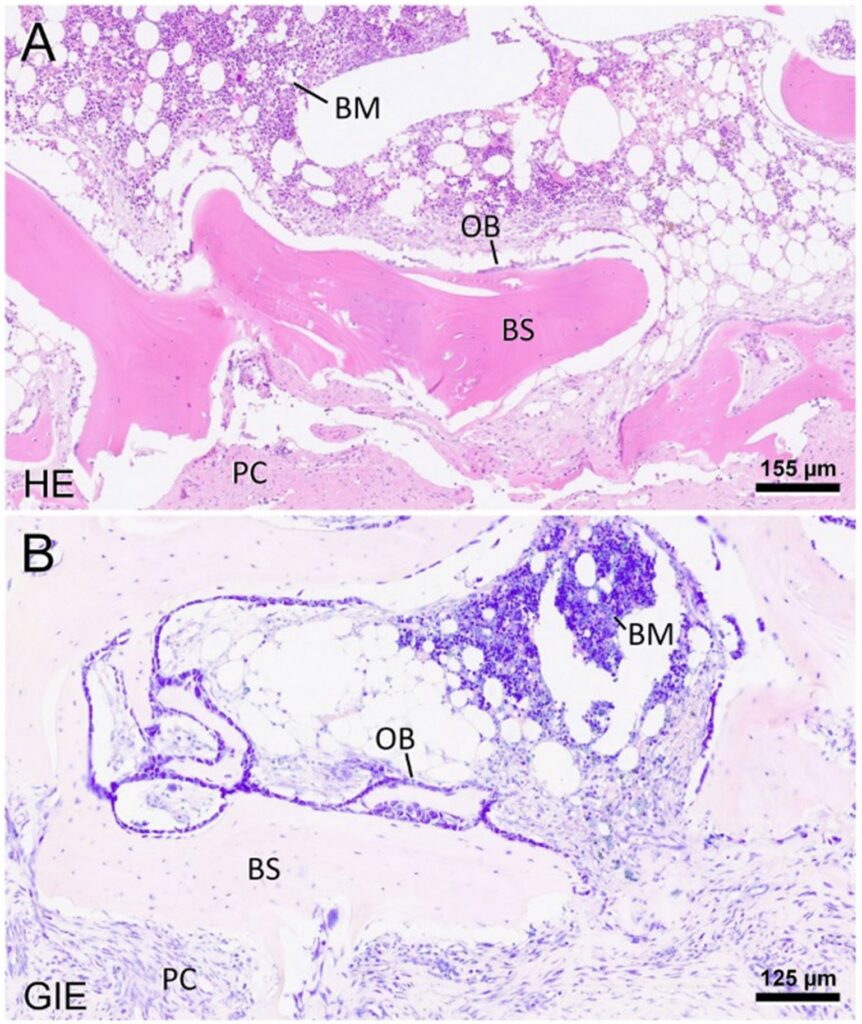
04 预后
术后X光检查发现了致密的残留组织(怀疑是坚硬囊的其余部分),证实异位骨化可能未被完全切除(下图)。
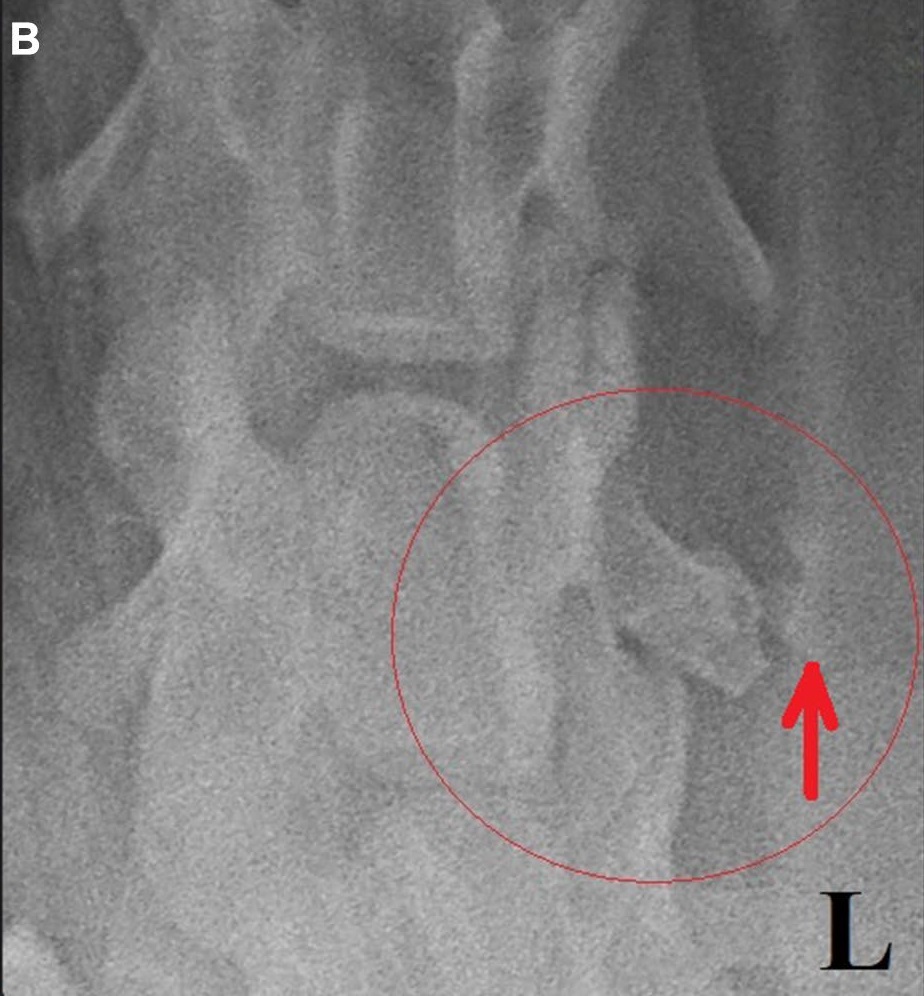
术后一个月内,跛行症状完全消失。
2年后,在手术部位的常规随访X光片上发现了一个8 mm大小的骨质病变,但没有相关的临床症状(下图)。这些随访时间点的神经系统检查结果均正常。
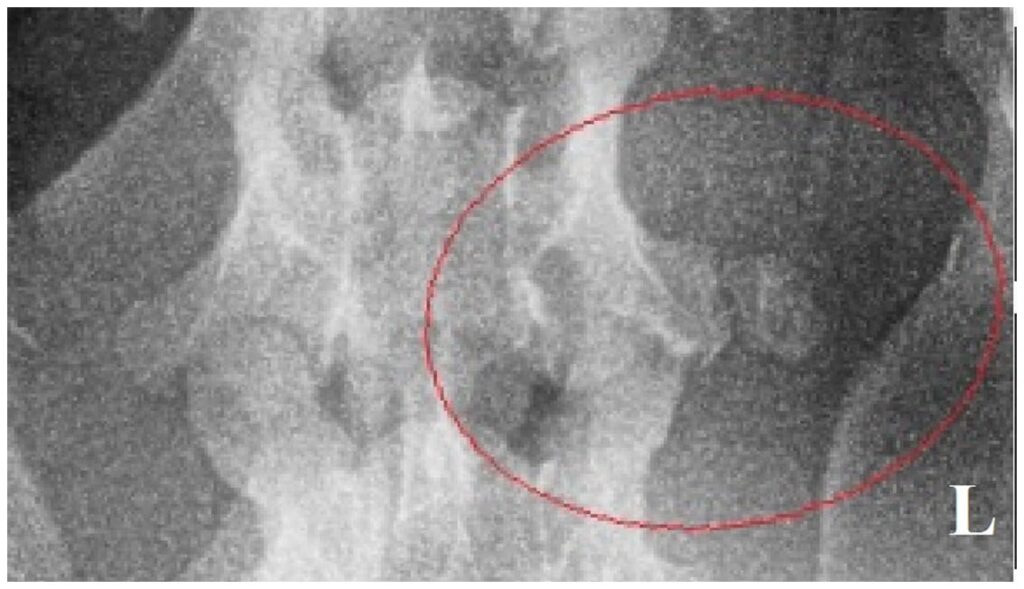
05 讨论
异位骨化(Heterotopic ossification,HO)又称副关节病、骨化性肌炎和异位钙化,是指在骨骼肌、关节囊、韧带和肌腱等软组织中异常形成成熟的片状骨[1-3]。
在人类医学中,HO主要分为两种类型——获得性和遗传性[4]。获得性HO最常见,75%的病例与组织创伤相关,可见于关节手术、肌肉骨骼或中枢神经系统损伤和烧伤后[5,6]。许多病例的病程是良性的,但也可能引起炎症、疼痛或功能性改变[7]。
在狗和猫中,HO的发病率很低,过去50年的病例报告也很少。在狗中,HO与髋关节周围的病变或创伤事件有关。在猫中,有类似人类病例的多灶性进行性纤维增生性病变的描述[8-21]。
在遗传性和获得性病例中,手术切除后复发的情况很常见,如本病例报告中所述的术后2年复发的情况。由于残留组织表明可能会重新生长,而且有可能复发,因此需要定期复查X光片。如有必要,将再次进行切除手术[20]。
狗患HO的情况很少见,大多数报告的病例都会影响髋关节和附着肌肉[9,10,21,22]。曾有类似报道称,一只跛行犬的颈椎附近出现了HO,但未提及与神经结构的联系[8]。
在本病例中,影像诊断与组织病理学的结合与人类医学中有关HO的报道一致。在人类的HO诊断过程中,会综合使用多种成像模式(CT、MRI和多普勒超声)。在本病例中,使用了X光片和MRI,成熟的HO在T1W和T2W图像上表现为由低密度皮质骨勾勒出的高密度松质骨脂肪,这可以被认为是诊断性的。
在本病例中,HO是在骨小梁形成的后期才被诊断出来的。在人类中,HO早期的放射学和组织学特征具有不同的特点。因此,当MRI检测到成熟期的HO时,就无需进行进一步的成像检查。
另一方面,HO早期阶段的MRI在排除其他鉴别诊断方面具有很大优势——识别HO的MRI模式在早期阶段非常有益,因为该病症通常会被误诊为骨髓炎或恶性肿瘤(如肉瘤)[23-26]。
组织学特征反映了放射学结果——早期病变显示出非常细胞化的丰满成纤维细胞片,细胞呈纺锤形或星状,似乎漂浮在类肌细胞外基质中。一周后,外围部分出现骨质接缝。在人类医学中,由于细胞密集并产生类骨质,处于这一演变阶段的病变被称为”软组织假恶性骨肿瘤”[27-29]。
尽管细胞度和有丝分裂率很高,但细胞学不典型性和异常有丝分裂并不存在。HO的一个特征是肿块外围部分的骨骼肌被卡住。6周后,肿块的外部显示出致密的片状骨,排列成假性皮质。6个月至1年后,演变为厚实、成熟的骨小梁。较老的病变也可能出现骨髓。
HO的并发症可能会导致邻近关节的活动受限,偶尔病变可能会侵犯邻近的神经,这种病理迄今仅在猫科动物和人类[11,30]中有所描述。
据推测,非遗传性HO的发病机制有四个必要因素[31]。
- 首先,必须有原发性损伤,通常是可能形成血肿的外伤。通常情况下,损伤程度很轻,仅由几条撕裂的肌肉或胶原纤维组成。
- 第二个因素是来自受伤部位的信号,这种信号很可能是受伤组织细胞分泌的蛋白质,或者是因组织受伤而到达的炎症细胞分泌的蛋白质。
- 第三,必须有间充质细胞的供应——合成类骨和软骨材料的基因被激活,使这些间充质细胞分化成成骨细胞或成软骨细胞——HO的形成可能发生在这些软组织的任何部位,包括骨骼肌、血管周围组织和纤维组织。
- 最后,必须存在有利于异位骨持续生成的必要环境。
在这四个因素中,信号因子似乎在异位骨的形成过程中扮演着最重要的角色,最近人类医学在了解这些因子方面取得了进展[4,32-37]。
这篇文章的主要局限性在于缺乏能直接证明神经卡压的直观证据,如术中图像或足以观察到神经的MRI成像细节。尽管如此,神经系统检查、MRI病灶定位、手术结果以及术后神经功能缺损的缓解都与本病例中描述的神经卡压相符。
文献来源:Hajek I, Rosati M, Matiasek K, Babinsky M, Caine A, Palus V. Case report: Focal heterotopic ossification in paravertebral muscles as a cause of neurogenic lameness in a dog. Front Vet Sci. 2024 May 23;11:1335175.
参考文献
1. Naraghi FF, DeCoster TA, Moneim MS, Miller RA, Rivero D. Heterotopic ossification. Orthopedics. (1996) 19:145–52.
2. Xu Y, Huang M, He W, He C, Chen K, Hou J, et al.. Heterotopic ossification: clinical features, basic researches, and mechanical stimulations. Front Cell Dev Biol. (2022) 10:770931.
3. Cipriano CA, Pill SG, Keenan MA. Heterotopic ossification following traumatic brain injury and spinal cord injury. J Am Acad Orthop Surg. (2009) 17:689–97.
4. Mujtaba B, Taher A, Fiala MJ, Nassar S, Madewell JE, Hanafy AK, et al.. Heterotopic ossification: radiological and pathological review. Radiol Oncol. (2019) 53:275–84.
5. Lipscomb AB, Thomas ED, Johnston RK. Treatment of myositis ossificans traumatica in athletes. Am J Sports Med. (1976) 4:111–20.
6. Kornhaber R, Foster N, Edgar D, Visentin D, Ofir E, Haik J, et al.. The development and impact of heterotopic ossification in burns: a review of four decades of research. Scars Burn Heal. (2017) 3:2059513117695659.
7. Popovic M, Agarwal A, Zhang L, Yip C, Kreder HJ, Nousiainen MT, et al.. Radiotherapy for the prophylaxis of heterotopic ossification: a systematic review and meta-analysis of published data. Radiother Oncol. (2014) 113:10–7.
8. Guilliard MJ. Fibrodysplasia ossificans in a German shepherd dog. J Small Anim Pract. (2001) 42:550–3.
9. Dueland RT, Wagner SD, Parker RB. von Willebrand heterotopic osteochondrofibrosis in Doberman pinschers: five cases (1980-1987). J Am Vet Med Assoc. (1990) 197:383–8.
10. Liu SK, Dorfman HD. A condition resembling human localized myositis ossificans in two dogs. J Small Anim Pract. (1976) 17:371–7.
11. Warren HB, Carpenter JL. Fibrodysplasia ossificans in three cats. Vet Pathol. (1984) 21:495–9.
12. Dillon EA. Traumatic myositis ossificans in a dog. N Z Vet J. (1988) 36:152–3.
13. Valentine BA, George C, Randolph JF, Center SA, Fuhrer L, Beck KA. Fibrodysplasia ossificans progressiva in the cat. A case report. J Vet Intern Med. (1992) 6:335–40.
14. Yabuzoe A, Yokoi S, Sekiguchi M, Momoi Y, Ide K, Nishifuji K, et al.. Fibrodysplasia ossificans progressiva in a Maine coon cat with prominent ossification in dorsal muscle. J Vet Med Sci. (2009) 71:1649–52.
15. Klang A, Kneissl S, Glänzel R, Fuchs-Baumgartinger A. Imaging diagnosis: fibrodysplasia ossificans progressiva in a cat. Vet Radiol Ultrasound. (2013) 54:532–5.
16. Asano K, Sakata A, Shibuya H, Kitagawa M, Teshima K, Kato Y, et al.. Fibrodysplasia ossificans progressiva-like condition in a cat. J Vet Med Sci. (2006) 68:1003–6.
17. Jacobsen KL, Wiebe V, Davidson AP, Murphy BG, Pool JRR. Use of Enrofloxacin and hydrotherapy in the Management of Fibrodysplasia Ossificans Progressiva (FOP) in a Savannah cat. Top Companion Anim Med. (2023) 52:100757.
18. Casal ML, Engiles JB, Zakošek Pipan M, Berkowitz A, Porat-Mosenco Y, Mai W, et al.. Identification of the identical human mutation in ACVR1 in 2 cats with Fibrodysplasia Ossificans Progressiva. Vet Pathol. (2019) 56:614–8.
19. Morton BA, Hettlich BF, Pool RR. Surgical treatment of traumatic myositis Ossificans of the extensor carpi Radialis muscle in a dog. Vet Surg. (2015) 44:576–80.
20. De Paolo M, Gracis M, Lacava G, Vapniarsky N, Arzi B. Management of bilateral pterygoid myositis ossificans-like lesion in dogs. Front Vet Sci. (2022) 9:992728.
21. Vilar JM, Ramirez G, Spinella G, Martinez A. Kinematic characteristics of myositis ossificans of the semimembranosus muscle in a dog. Can Vet J. (2010) 51:289–92.
22. Tambella AM, Palumbo Piccionello A, Dini F, Vullo C, Rossi G, Scrollavezza P. Myositis ossificans circumscripta of the triceps muscle in a Rottweiler dog. Vet Comp Orthop Traumatol. (2013) 26:154–9.
23. Zagarella A, Impellizzeri E, Maiolino R, Attolini R, Castoldi MC. Pelvic heterotopic ossification: when CT comes to the aid of MR imaging. Insights Imaging. (2013) 4:595–603.
24. Choi YH, Kim KE, Lim SH, Lim JY. Early presentation of heterotopic ossification mimicking pyomyositis – two case reports. Ann Rehabil Med. (2012) 36:713–8.
25. Siegel MJ. Magnetic resonance imaging of musculoskeletal soft tissue masses. Radiol Clin North Am. (2001) 39:701–20.
26. Chan WP. Magnetic resonance imaging of soft-tissue tumors of the extremities: a practical approach. World J Radiol. (2013) 5:455–9.
27. Ogilvie-Harris DJ, Fornasier VL. Pseudomalignant myositis ossificans: heterotopic new-bone formation without a history of trauma. J Bone Joint Surg Am. (1980) 62:1274–83.
28. Lagier R, Cox JN. Pseudomalignant myositis ossificans. A pathological study of eight cases. Hum Pathol. (1975) 6:653–65.
29. Kaplan FS, Gannon FH, Hahn GV, Wollner N, Prauner R. Pseudomalignant heterotopic ossification. Clin Orthop Relat Res. (1998) 346:134–40.
30. McCarthy EF, Sundaram M. Heterotopic ossification: a review. Skeletal Radiol. (2005) 34:609–19.
31. Kaplan FS, Glaser DL, Hebela N, Shore EM. Heterotopic ossification. J Am Acad Orthop Surg. (2004) 12:116–25.
32. Urist MR. Bone: formation by autoinduction. Science. (1965) 150:893–9.
33. Kaplan FS. Skin and bones. Arch Dermatol. (1996) 132:815–8.
34. Kingsley DM. The TGF-beta superfamily: new members, new receptors, and new genetic tests of function in different organisms. Genes Dev. (1994) 8:133–46.
35. Wozney JM, Rosen V, Byrne M, Celeste AJ, Moutsatsos I, Wang EA. Growth factors influencing bone development. J Cell Sci Suppl. (1990) 1990:149–56.
36. Jones CM, Lyons KM, Hogan BL. Involvement of bone morphogenetic Protein-4 (BMP-4) and Vgr-1 in morphogenesis and neurogenesis in the mouse. Development. (1991) 111:531–42.
37. Nakase T, Nomura S, Yoshikawa H, Hashimoto J, Hirota S, Kitamura Y, et al.. Transient and localized expression of bone morphogenetic protein 4 messenger RNA during fracture healing. J Bone Miner Res. (1994) 9:651–9.