
| 品种:澳洲牧羊犬 | |
| 年龄:4岁 | |
| 性别:雌 | |
| 诊断:白塞氏病 | |
01 主诉及病史
4个月前出现腹腔积气、发热和中性粒细胞减少。尽管服用了几个疗程的抗生素和一个疗程的美洛昔康,仍持续发烧。
4天前,眼部出现绿色分泌物并高烧不退(直肠温度41.3°C [37.5-39.2])。急诊就诊后发现了低蛋白血症、中性粒细胞减少和轻微的电解质紊乱。出院后再次出现厌食和呕吐。第二次急诊拍片发现腹腔积气(下图)。
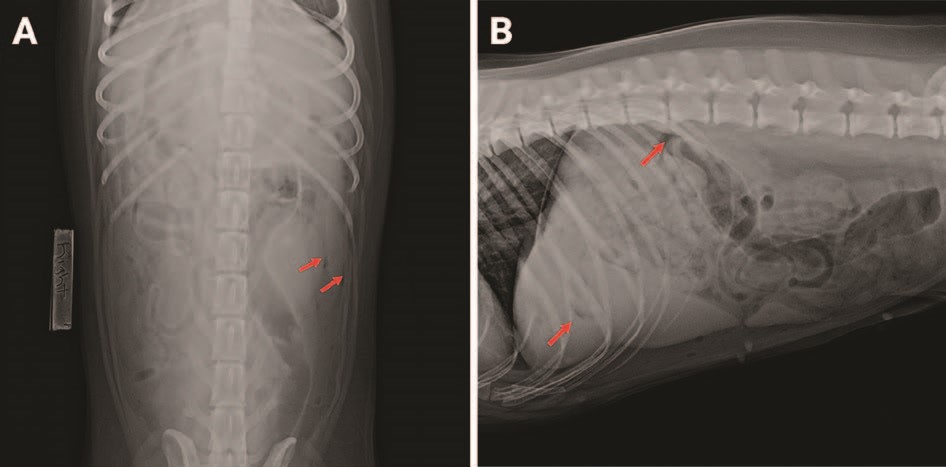
02 检查
体重14.9千克。神志清楚、反应灵敏,但有轻度心动过速(140次/分 [70-120])和发热(直肠温度39.3°C [37.5-39.2])。下唇出现溃疡,腹部触诊时疼痛,直肠指检发现有血迹。
初步血检结果与之前的结果相似,包括严重的持续性中性粒细胞减少。腹部超声显示有中等量的游离气体和结肠壁周缘增厚的病灶(下图)。这些结果都表明可能存在脓毒性腹膜炎,需要急诊剖腹探查术。
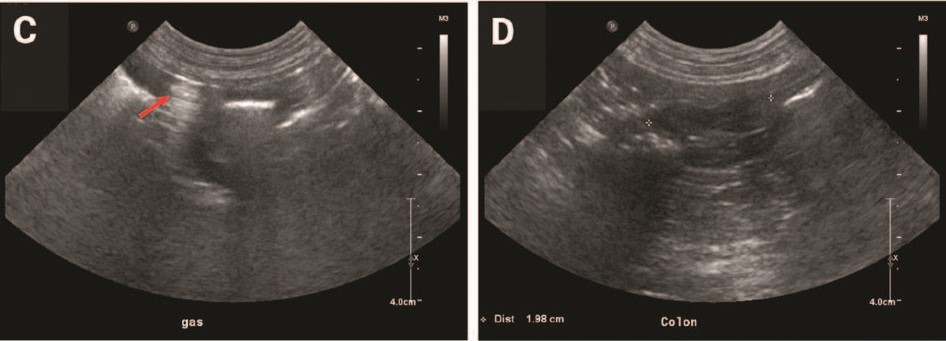
↑ 腹部超声证实存在游离气体(C;红色箭头),并发现结肠周壁增厚区域(D)。
其他诊断结果包括抗核抗体血清学阴性、多药耐药性1基因正常、基线皮质醇略微升高(4.7 μg/dL [1.8-4.0])、血清钴胺素正常(581 pg/mL [175-800])、粪便浮选检查未发现肠道寄生虫。中性粒细胞减少的遗传原因也在考虑之列,但根据品种、年龄和不一致的临床特征排除了这些可能的鉴别诊断。
03 手术
术中发现远端降结肠全层穿孔(下图),部分被网膜覆盖。穿孔附近有一个溃疡灶,沿空肠和回肠的肠管前缘有10-12个圆形、红色、隆起的病灶。脾脏囊膜表面呈斑驳白色,有多灶性网膜粘连。
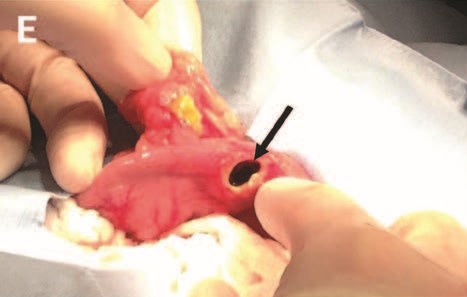
↑ 降结肠远端全层穿孔(箭头)。
进行了结肠部分切除术。切除的远端降结肠部分、具有代表性的空肠和网膜活检样本以及整个脾脏都被固定并送去做常规组织病理学检查。
空肠和结肠的网膜和穿孔表面样本显示出纤维素性腹膜炎和化脓性腹膜炎的特征。空肠和切除的结肠样本显示急性粘膜溃疡,伴有跨膜穿孔和嗜中性组织细胞性小肠结肠炎(下图)。溃疡下方的结肠粘膜下层显示多灶性白细胞凝集性血管炎,动脉血管壁纤维素性坏死,间质渗出大量白细胞和纤维蛋白,扩张的淋巴管充满水肿液。溃疡空肠内的早期肉芽组织表明,这种病变发生在结肠穿孔之前。脾脏的组织病理学结果正常。
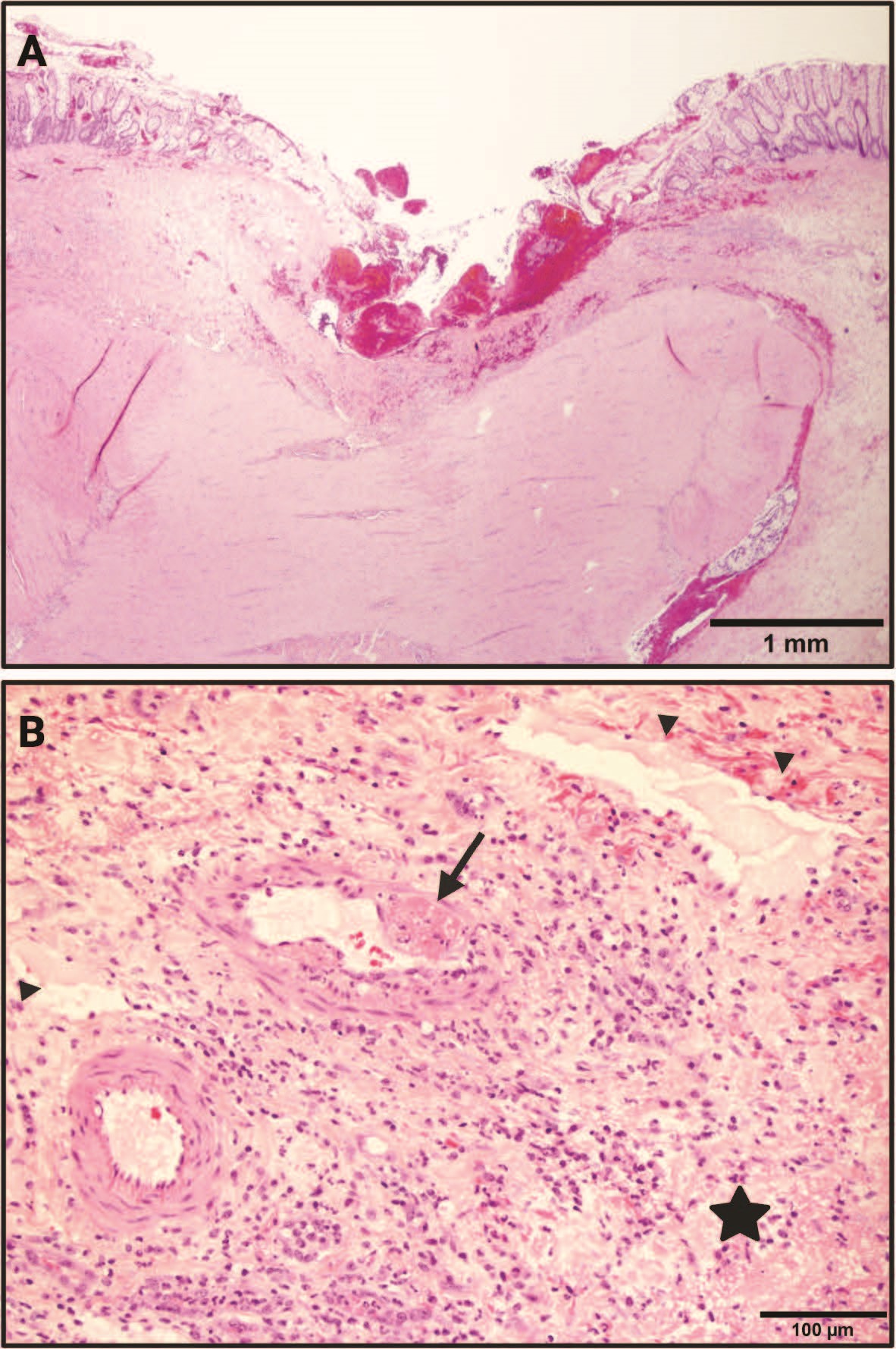
↑ (A)结肠粘膜溃疡,伴有局部广泛的急性粘膜下水肿和出血。(B)溃疡下方的结肠粘膜下层,显示白细胞凝集性血管炎和动脉血管壁纤维素性坏死(箭头)、间质白细胞和纤维蛋白渗出(星号)以及充满水肿液的扩张淋巴管(箭头)。
04 预后
术后处理包括抗生素、止痛、对症药物和静脉输液。
术后第2天,舌头腹侧、下唇和左上口腔粘膜又出现了多处阿弗他溃疡(下图)。导管部位近端还出现了静脉炎。在整个住院期间,一直间歇性发烧(直肠温度38.4-41.3°C)。
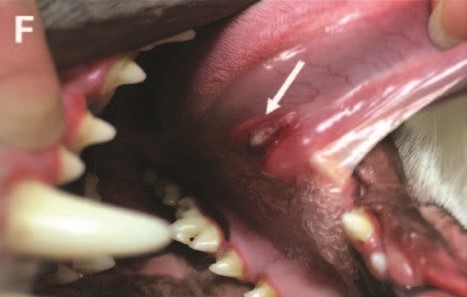
↑ 舌阿弗他溃疡照片(白色箭头)。
术后第3天,身上出现了几个非溃疡性皮肤结节。切除了其中2个结节,病理学发现局部广泛的化脓性泛发性炎(下图),伴有多灶性皮下白细胞凝集性血管炎和血管壁纤维素性坏死,主要影响毛细血管,也影响小口径动脉和静脉。鉴于发现了血管炎,其他组化染色没有发现明显的病原体,术后5天开始使用地塞米松(0.05 mg/kg,IV,q24h)。
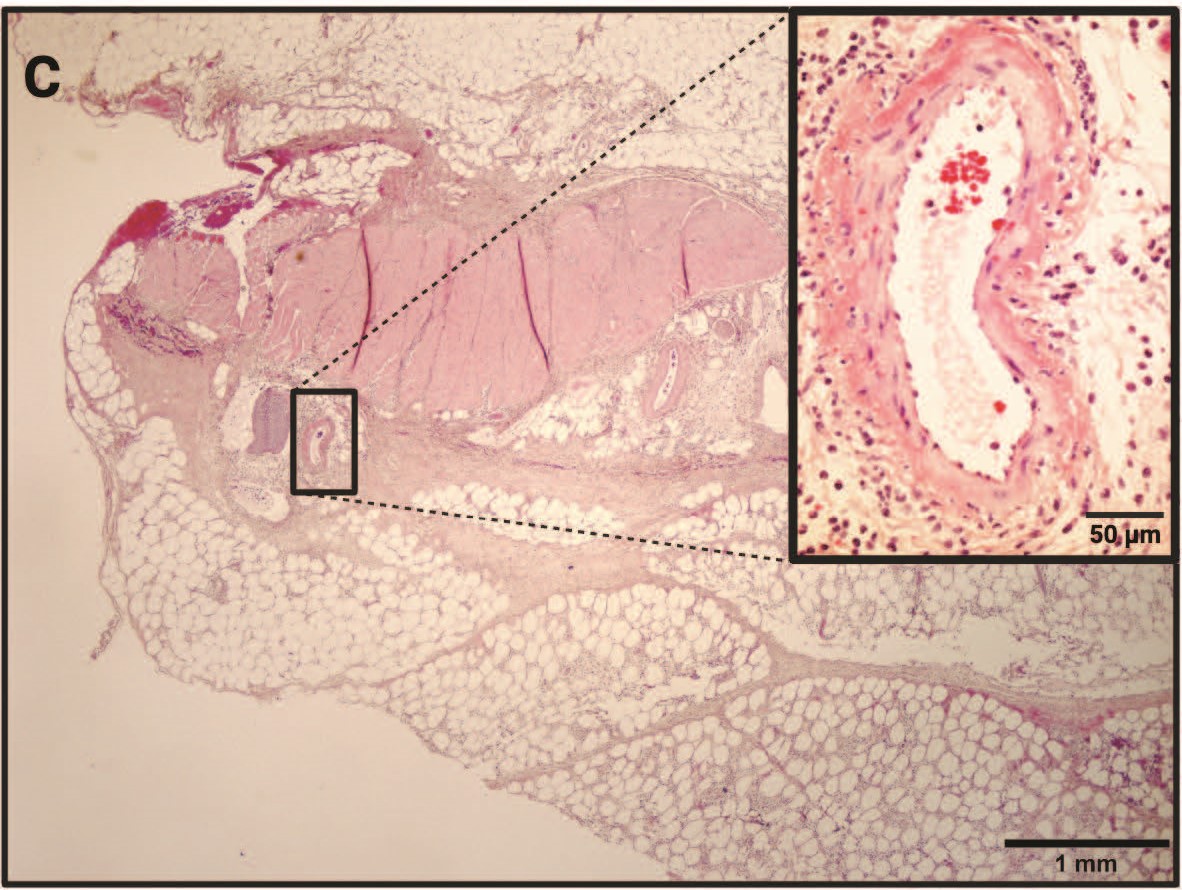
↑ 局部广泛急性化脓性泛发性皮肤皮下组织。放大图:皮下动脉血管壁的白细胞凝集性血管炎和纤维素性坏死。
术后第6天,左眼出现中度结膜炎和充血,伴有视物模糊。没有发现角膜溃疡,但左眼结膜出现了溃疡。右眼眼压16 mmHg,左眼眼压11 mmHg。支持左眼葡萄膜炎的诊断。
术后第7天,出院,出院时服用泼尼松(1 mg/kg,PO,q24h)、多种抗生素、治疗葡萄膜炎的眼科药物和辅助药物。
出院后3天,体温正常,葡萄膜炎和结膜炎已缓解。中性粒细胞减少基本缓解。
出院后9天,因呕吐、厌食和腹痛再次就诊。直肠温度39.4°C,心动过速(176 次/分)。之前的导管位置出现了破裂的脓疱。超声发现了少量的游离腹腔积液,腹腔积液细胞学检查未发现传染性病菌。
接受了输液治疗,并在晶体液和芬太尼作用下住院。进一步检查发现腹腔积液主要由未变性的中性粒细胞、单核细胞和巨噬细胞组成,中性粒细胞和巨噬细胞内含有细胞内球菌。许多巨噬细胞含有细胞质内的革兰氏阴性包涵体,与酵母菌最为一致。这些发现促使患者进行了第二次探查性开腹手术。在十二指肠近端入口附近的胆总管上发现了一处撕裂,并进行了手术修复。
第二次开腹手术和胆管修复术后,接受了泼尼松(1 mg/kg,PO,q24h)、霉酚酸(10 mg/kg,PO,q12h)以及抗菌药和支持性药物治疗。术后住院6天。除了D-二聚体升高(2,698 ng/mL [0-575])外,凝血功能检查没有异常。出院时服用了泼尼松、霉酚酸、抗菌素和镇痛剂。
第二次术后2个月内,临床状况有所缓解。泼尼松在3个月内逐渐减量至每天0.3 mg/kg,最后减至隔天0.3 mg/kg。每天继续服用霉酚酸。后续失去了随访。
05 讨论
白塞氏病(Behçet disease)也被称为贝赫切特综合征,通常表现为口腔溃疡、生殖器溃疡和血管炎引起的葡萄膜炎。这种罕见的慢性炎症性疾病的特点是多系统受累和免疫介导的发病机制。本病例没有生殖器溃疡,而且并非所有人类病例都会出现生殖器溃疡。
值得注意的是,一些白塞氏病患者会出现肠溃疡,并伴有出血或穿孔[1] ,就像本病例一样。此外,本病例的一些临床症状没有反复发作的记录,这也是白塞氏病的一个考虑因素。不过,本病例的临床特征与白塞氏病非常相似,这表明狗也会患上类似的疾病。主要相似之处包括以下几点:
反复发烧和溃疡:患者持续发烧,对抗生素无反应,并出现口腔和肠道溃疡。同样,白塞氏病也以反复发烧和粘膜病变为特征。
全身性血管炎:皮肤结节和肠道的组织病理学评估显示,血管炎伴有白细胞增生和纤维素性坏死,与免疫复合物沉积一致。白塞氏病也以全身性血管炎为特征,组织学结果与此相似[2]。白塞氏病也会出现结节性红斑样泛发性炎[3],与本病例中观察到的泛发性炎相似[4]。
胃肠道表现: 患者的空肠和结肠出现多灶性溃疡,结肠穿孔导致腹膜炎。白塞氏病的胃肠道特征通常包括溃疡和炎症,这些溃疡和炎症可导致穿孔和严重的并发症[1]。白塞氏病患者的另一个胃肠道症状是直肠出血,这只狗就是如此。
眼部受累:本患者的葡萄膜炎是人类白塞氏病的特征之一。
对免疫调节的反应:本患者对强的松和霉酚酸等免疫抑制疗法的反应支持了潜在的免疫介导发病机制。白塞氏病也需要使用免疫抑制剂来控制多器官血管炎和泛发性炎症。
对该患者使用免疫抑制剂、抗生素和支持性护理,这与白塞氏病患者的治疗方案一致,即进行免疫调节和对症治疗[5]。由于复发有可能导致危及生命的并发症,因此选择了保守性泼尼松减量和无限期使用霉酚酸。
总之,本病例强调了在动物中出现多系统血管炎和炎症体征时考虑免疫介导性疾病的重要性。该病例与人类的白塞氏病相似,建议考虑在有类似症状的犬中关注白塞氏病的发生。
文献来源:Yao A, Loftus JP, Duhamel GE, Center SA, Ash K, Thompson M. An Australian Shepherd with possible Behçet-like disease characterized by cutaneous and intestinal vasculitis leading to septic abdomen. J Am Vet Med Assoc. 2024 Oct 18;263(1):1-4.
参考文献
1. Hatemi I, Hatemi G, Çelik AF. Systemic vasculitis and the gut. Curr Opin Rheumatol. 2017;29(1):33-38.
2. Adil A, Goyal A, Quint JM. Behcet disease. In: StatPearls. StatPearls Publishing; 2024. Accessed May 23, 2024.
3. Kim B, LeBoit PE. Histopathologic features of erythema nodosum-like lesions in Behçet disease: a comparison with erythema nodosum focusing on the role of vasculitis. Am J Dermatopathol. 2000;22(5):379-390.
4. International Team for the Revision of the International Criteria for Behçet’s Disease (ITR-ICBD). The International Criteria for Behçet’s Disease (ICBD): a collaborative study of 27 countries on the sensitivity and specificity of the new criteria. J Eur Acad Dermatol Venereol. 2014;28(3):338-347.
5. Alibaz-Oner F, Direskeneli H. Advances in the treatment of Behcet’s disease. Curr Rheumatol Rep. 2021;23(6):47.