
 | 品种:迷你松狮犬 |
| 年龄:5岁 | |
| 性别:雄 | |
| 诊断:外伤 | |
01 主诉及病史
左前胸有一个大裂口,肌肉分层暴露在外。
最初在另一家医院治疗,注射了镇静剂,对扩大的裂口进行了手术清创,并放置了引流管。2天后伤口开裂,引流管被拔除。医生建议对伤口进行二次手术清创,定期更换绷带,主人没有接受这一建议。
02 治疗
3天后,在未使用麻醉或镇静剂的情况下,用无菌生理盐水大量冲洗了伤口,并进行了首次异体富血小板纤维蛋白(PRF)治疗。
捐献PRF的狗生活在室内,通过免疫荧光抗体进行了筛查,接种了利什曼原虫疫苗,定期进行体内和体外驱虫,并及时接种疫苗。被选为捐献犬期间或之前的15天内没有接种过任何疫苗或服用过任何药物。捐献犬在捐献前接受了临床评估,健康状况良好。
在剪毛并对穿刺部位进行消毒清洁后,从颈静脉抽取5毫升血液,将血液转移到不含凝血活化剂的57×15.3毫米无菌管中,立即在室温下以3000 rpm离心10分钟。离心结束后,血液在管内静置60分钟。使用无菌材料将PRF凝结块从试管中取出,去除红色部分,得到PRF(白色部分),准备局部移植到伤口中。
在每次移植PRF前,立即用无菌的0.9%生理盐水冲洗皮损,并用无菌纱布擦干。每次PRF治疗都是将新生产的PRF应用于病变区域,确保血小板和白细胞丰富的凝块区域与皮损接触。PRF结束后,使用无菌凡士林纱布和干绷带进行封闭包扎。使用PRF的数量取决于每个伤口的大小。约每2.5平方厘米的伤口表面使用一个PRF凝结块。
一旦肉芽组织覆盖了伤口,即伤口收缩并开始上皮化,则暂停使用PRF。一直使用无菌凡士林纱布和干绷带进行包扎,直到伤口完全闭合。在暂停PRF治疗到伤口完全闭合期间,只使用干纱布覆盖伤口。当伤口出现坚实的小结痂,表明已进入后期恢复阶段时,才暂停使用干纱布。
使用克林霉素(11 mg/kg PO q24h,15天)、卡泊芬(2 mg/kg PO q24h,5天)。在住院的前24小时内接受了美沙酮(0.3 mg/kg IV q12h),之后5天改为曲马多(3 mg/kg PO q12h)。
03 预后
第1天,感染伤口的初始面积为16.12平方厘米。第7天,经过一周的PRF治疗后,伤口面积为6.67平方厘米。第10天和第17天,伤口面积分别为2.80平方厘米和0.68平方厘米。1个月后,进行了3次PRF治疗和2次干纱布换药,直至伤口完全闭合(下图)。使用弹性绷带将伤口固定在身体周围。

| 病例2 | |
|---|---|
 | 品种:混种犬 |
| 年龄:10岁 | |
| 性别:雌 | |
| 体重:9.5千克 | |
| 诊断:外伤 | |
04 主诉及病史
遭遇道路交通事故,后肢出现大面积撕裂伤,外侧副韧带外露,出现组织缺损。
患者出现疼痛并伴有单侧耻骨骨折,经药物治疗后病情稳定。急诊室使用无菌生理盐水冲洗伤口,并用封闭绷带保护伤口。2天后,进行了皮肤裂伤矫正手术。由于组织损失严重,韧带外露,因此无法通过手术完全闭合创面。医生建议在第二次手术中进行植皮,并通过更换绷带进行伤口管理,直到可以进行植皮为止。由于植皮可能会出现并发症,主人拒绝了这一建议。
05 治疗
PRF治疗在术后第1天开始,也就是车祸4天后进行。病变部位水肿并有纤维蛋白沉积,面积为6.22平方厘米。
接受了阿莫西林-克拉维酸(20 mg/kg PO q12h,10天)、美洛昔康(0.1 mg/kg PO q24h,5天)。在住院的前48小时内接受了美沙酮(0.3 mg/kg IV q12h)以及曲马多(3 mg/kg PO q12h,5天)。
06 预后
第1周,病灶接受了3次PRF治疗,之后每周治疗一次,直至完全愈合。第12天,伤口面积缩小到3.58平方厘米。第26天,伤口面积为1.44平方厘米。1个月后,伤口面积为0.88平方厘米。共使用了5次PRF治疗及3次干纱布换药,经过47天的治疗后,伤口完全闭合(下图)。
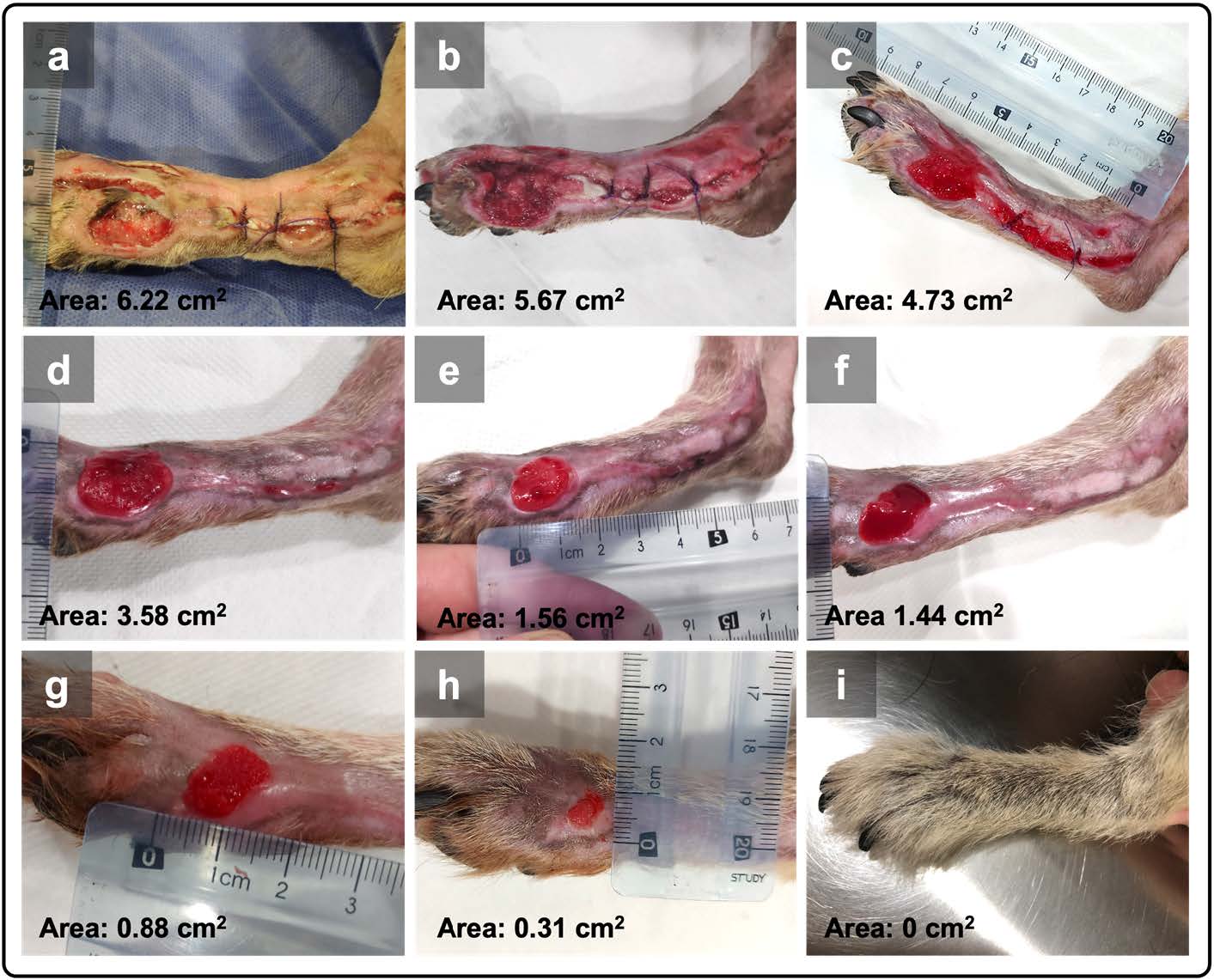
两例患者能很好地耐受反复的伤口处理,包括PRF移植和绷带更换,无需使用局部镇痛药。在异体PRF治疗后的至少4个月内,伤口愈合美观且顺利,没有出现伤口复发或局部改变。
07 讨论
本文报告了使用异体富血小板纤维蛋白(platelet-rich fibrin,PRF)治疗两只小型犬自然形成的伤口的情况。PRF疗法涉及血液衍生物的使用,被定义为一种有效且经济的伤口愈合生物疗法。PRF疗法在人类医学中的报道越来越多。兽医领域有关异体PRF疗法的报道很少,但目前正在试用这种疗法。自体
PRF疗法在人类和兽医领域均有报道,但在某些患者中可能存在一些局限性,尤其是那些无法进行采血的患者[1-3]。
PRF被定义为一种生物相容性和可生物降解的血液衍生物,由天然纤维蛋白支架组成,其中含有升高的血小板和白细胞聚集体,并释放出高浓度的生物活性生长因子和细胞因子[4,5]。这些生长因子通过激活细胞内信号通路,在调节和调控细胞活动方面发挥着核心作用,导致局部细胞增殖、分化或凋亡,甚至导致介入细胞分泌其他蛋白质,产生旁分泌效应[6]。
在皮肤修复过程中,成纤维细胞、内皮细胞和角质形成细胞的增殖发生在受伤区域内几个常驻和招募的细胞元素之间复杂的分子串联中[7]。此外,其他研究也发现了PRF疗法的抗菌、消炎和镇痛作用[8,9]。
异体血小板制剂,如PRF和富血小板血浆(另一种著名的血小板血液制剂)的免疫原性在有关异体治疗的人体临床描述中未得到证实。在不考虑血型鉴定或交叉配血检查的情况下,使用异体血小板血液制剂未出现全身或局部不良免疫反应[23,24,25]。
在本病例报告中,PRF疗法最重要的目标是减少就诊次数,降低更换绷带的频率。传统治疗方法需要每隔3-4天更换一次绷带,同时采用药物治疗并进行伤口处理,直到伤口闭合为止[19]。两例患者在接受PRF治疗前均接受过手术伤口处理,但均以失败告终:病例1伤口开裂;病例2由于组织严重缺损,伤口无法完全闭合。应用PRF疗法可以减少对伤口的操作和就诊次数。
总之,PRF疗法是一种生物再生策略,适用于兽医实践中的伤口管理。PRF凝结块作为一种移植技术直接应用于伤口,起到促进再生的作用。当由于各种原因(经济限制、需要手术清创时麻醉风险增加等)需要第二次愈合意向时,它还提供了一种替代技术。此外,在治疗过程中没有使用抗菌剂,这表明PRF疗法有利于伤口护理的环境。要全面评估PRF在犬伤口治疗中的潜在益处,还需要进一步的对照组研究。
文献来源:Soares CS, Dias IR, Barros LC, Carvalho PP, Pires MDA. Translational Clinical Research: Use of Allogeneic Platelet-Rich Fibrin (PRF) for Wound Regeneration in Two Small-Sized Dogs. Animals (Basel). 2025 Jan 27;15(3):367.
参考文献
1.Chung T., Baek D., Kim N., Park J., Park C. Topical allogeneic platelet-rich plasma treatment for a massive cutaneous lesion induced by disseminated intravascular coagulation in a toy breed dog. Ir. Vet. J. 2015;68:4.
2.Soares C.S., Barros L.C., Saraiva V., Gomez-Florit M., Babo P.S., Dias I.R., Reis R.L., Carvalho P.P., Gomes M.E. Bioengineered surgical repair of a chronic oronasal fistula in a cat using autologous platelet-rich fibrin and bone marrow with a tailored 3D printed implant. J. Feline Med. Surg. 2018;20:835–843.
3.Soares C.S., Dias I.R., Pires M.A., Carvalho P.P. Canine-Origin Platelet-Rich Fibrin as an Effective Biomaterial for Wound Healing in Domestic Cats: A Preliminary Study. Vet. Sci. 2021;8:213.
4.Pinto N.R., Ubilla M., Zamora Y., Del Rio V., Dohan Ehrenfest D.M., Quirynen M. Leucocyte- and platelet-rich fibrin (L-PRF) as a regenerative medicine strategy for the treatment of refractory leg ulcers: A prospective cohort study. Platelets. 2018;29:468–475.
5.Soares C.S., Babo P.S., Faria S., Pires M.A., Carvalho P.P. Standardized Platelet-Rich Fibrin (PRF) from canine and feline origin: An analysis on its secretome pattern and architectural structure. Cytokine. 2021;148:155695.
6.Margono D.A., Bagio D.A., Nursasongko B., Nazar K., Yulianto I., Gayatri E., Lengah D., Megantoro A. Comparison of Advanced Platelet Rich Fibrin (A-PRF) and Culture Media Conditioned Warton’s Jelly (CMCWJ) on Fibroblast Cells Proliferation. Pesqui. Bras. Odontopediatria Clin. Integr. 2018;18:1–9.
7.Tottoli E.M., Dorati R., Genta I., Chiesa E., Pisani S., Conti B. Skin Wound Healing Process and New Emerging Technologies for Skin Wound Care and Regeneration. Pharmaceutics. 2020;12:735.
8.Ozgul O., Senses F., Er N., Tekin U., Tuz H.H., Alkan A., Kocyigit I.D., Atil F. Efficacy of platelet rich fibrin in the reduction of the pain and swelling after impacted third molar surgery: Randomized multicenter split-mouth clinical trial. Head Face Med. 2015;11:37.
9.Shariati A., Moradabadi A., Azimi T., Ghaznavi-Rad E. Wound healing properties and antimicrobial activity of platelet-derived biomaterials. Sci. Rep. 2020;10:1032.
10.Soares C.S., Dias I.R., Barros L.C., Pires M.d.A., Carvalho P.P. Management of canine wounds using platelet-rich fibrin (PRF) biomaterial. A case series report. Vet. Med. Sci. 2024;10:e1236.
11.Maghsoudi O., Ranjbar R., Mirjalili S.H., Fasihi-Ramandi M. Inhibitory activities of platelet-rich and platelet-poor plasma on the growth of pathogenic bacteria. Iran. J. Pathol. 2017;12:79–87.
12.Feng M., Wang Y., Zhang P., Zhao Q., Yu S., Shen K., Miron R.J., Zhang Y. Antibacterial effects of platelet-rich fibrin produced by horizontal centrifugation. Int. J. Oral Sci. 2020;12:32.
13.Crisci A., Manfredi S., Crisci M. The L-PRF Membrane (Fibrin Rich in Platelets and Leukocytes) And Its Deriva- tives Useful as A Source of Stem Cells in Wound Surgery. J. Stem Cell Rep. 2019;1:1–11.
14.Attili A.-R., Iacoucci C., Serri E., Cuteri V., Cantalamessa A., Linardi M., Rifici C., Mazzullo G., Rossi G., Galosi L., et al. Antibacterial Properties of Canine Platelet-Rich Plasma and Other Non-Transfusional Hemo-Components: An in vitro Study. Front. Vet. Sci. 2021;8:746809.
15.Martínez C.E., González S.A., Palma V., Smith P.C. Platelet Poor Plasma and Platelet Rich Plasma Stimulate Bone Lineage Differentiation in Periodontal Ligament Stem Cells. J. Periodontol. 2015;87:e18–e26.
16.Miron R.J., Fujioka-Kobayashi M., Bishara M., Zhang Y., Hernandez M., Choukroun J. Platelet-Rich Fibrin and Soft Tissue Wound Healing: A Systematic Review. Tissue Eng. Part B Rev. 2017;23:83–99.
17.Ozer K., Colak O. Leucocyte- and platelet-rich fibrin as a rescue therapy for small-to-medium-sized complex wounds of the lower extremities. Burn. Trauma. 2019;7:11.
18.Hamed M.A., Abouelnasr K.S., El-Adl M., Abo Elfadl E.A., Farag A., Lashen S. Effectiveness of Allogeneic Platelet-Rich Fibrin on Second-Intention Wound Healing of Experimental Skin Defect in Distal Limb in Donkeys (Equus asinus) J. Equine Vet. Sci. 2019;73:131–138.
19.Gemignani F., Perazzi A., Iacopetti I. Use of canine sourced platelet-rich plasma in a feline contaminated cutaneous wound. Can. Vet. J. 2017;58:141–144.
20.Kuffler D. Variables affecting the potential efficacy of PRP in providing chronic pain relief. J. Pain Res. 2018;12:109–116.
21.Burnouf T., Chou M.-L., Lundy D.J., Chuang E.-Y., Tseng C.-L., Goubran H. Expanding applications of allogeneic platelets, platelet lysates, and platelet extracellular vesicles in cell therapy, regenerative medicine, and targeted drug delivery. J. Biomed. Sci. 2023;30:79.
22.Wardrop K.J., Birkenheuer A., Blais M.C., Callan M.B., Kohn B., Lappin M.R., Sykes J. Update on Canine and Feline Blood Donor Screening for Blood-Borne Pathogens. J. Vet. Intern. Med. 2016;30:15–35.
23.Liao X., Liang J.-X., Li S.-H., Huang S., Yan J.-X., Xiao L.-L., Song J.-X., Liu H.-W. Allogeneic Platelet-Rich Plasma Therapy as an Effective and Safe Adjuvant Method for Chronic Wounds. J. Surg. Res. 2020;246:284–291.
24.Semenič D. Regeneration of Chronic Wounds with Allogeneic Platelet Gel versus Hydrogel Treatment: A Prospective Study. Acta Clin. Croat. 2018;57:434–442.
25.Chen T.M., Tsai J.C., Burnouf T. A novel technique combining platelet gel, skin graft, and fibrin glue for healing recalcitrant lower extremity ulcers. Dermatol. Surg. 2010;36:453–460.