| 品种:短毛猫 | |
| 年龄:7岁 | |
| 性别:雌 | |
| 诊断:巴尔通体病 | |
01 主诉及病史
两天前出现呼吸困难、厌食和嗜睡症状。
以前未患任何疾病,逆转录病毒呈阴性。家中的另一只猫两周前因发烧住进本院,其血液巴尔通体PCR呈阳性。两只猫的生活方式都是室内或室外皆可。
02 检查
粘膜苍白,心脏有二级杂音,呼吸轻度受限(40次/分),心跳170次/分,发热(39.5°C),嗜睡,有明显的跳蚤感染。血液化验显示轻度正常红细胞性非再生性贫血(红细胞压积22.4%),血生化未发现异常。
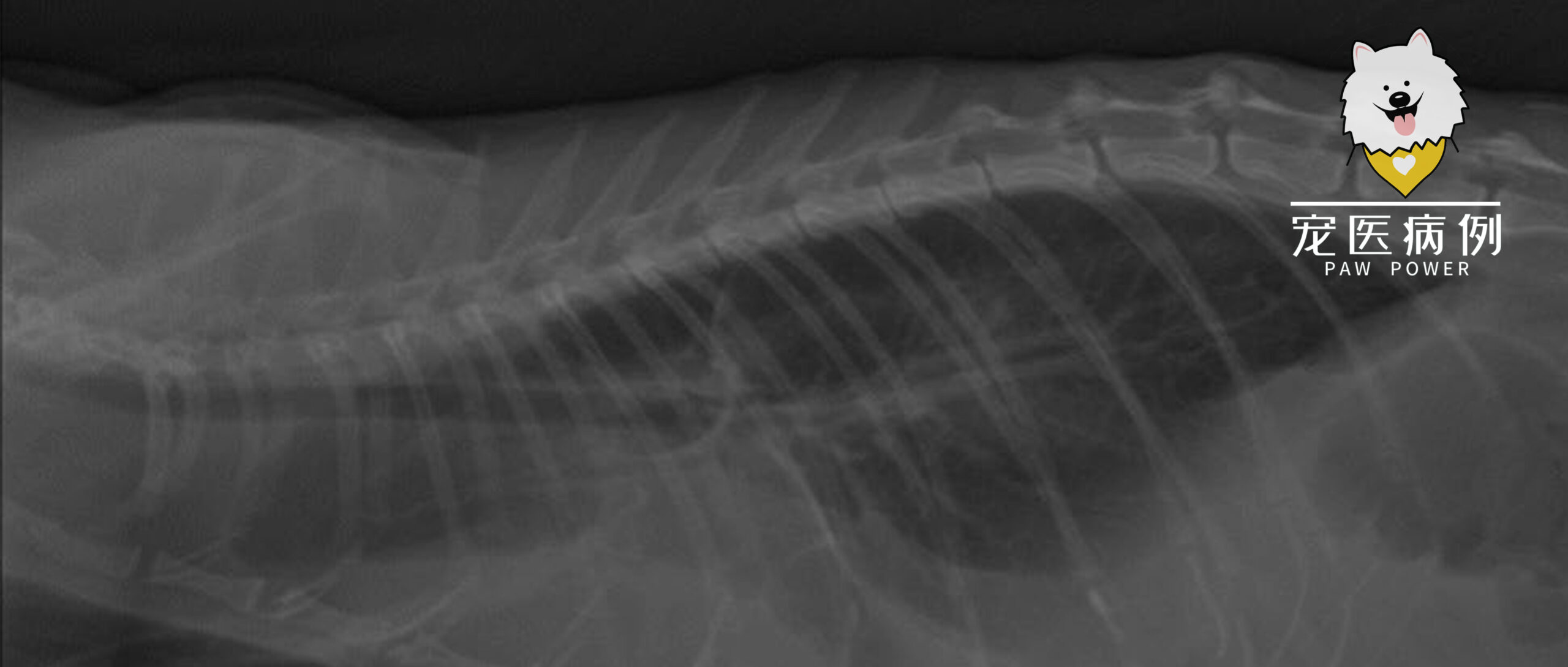
胸片显示有中度胸腔积液(下图)。

↑ 右侧胸片显示胸腔积液。
超声心动图显示有明显的心包积液和心包填塞(下图)。腹部超声显示轻度腹水,但无法采样。
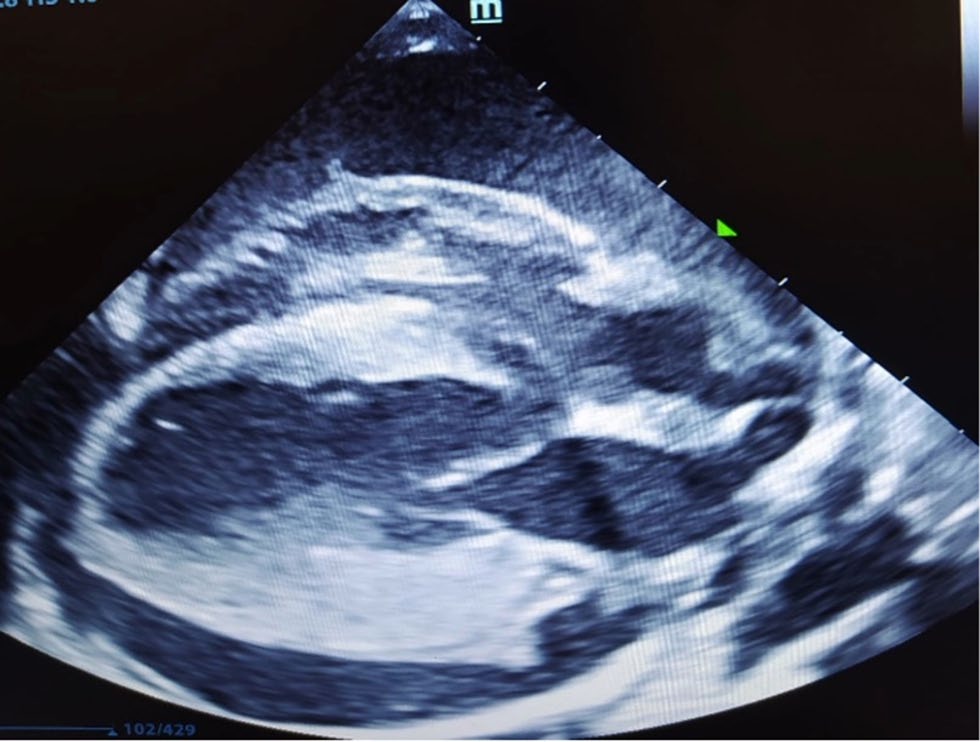
↑ 超声心动图显示心包积液。
镇静后进行心包穿刺和胸腔穿刺。首次心包穿刺时获得了少量样本,仅够进行体液分析和细胞学检查。随后心包积液消退,可能是由于心包积液排入了胸膜腔。随后进行了胸腔穿刺术,获得了50毫升积液。积液中的有核细胞计数和蛋白质浓度与富含蛋白质的渗出液一致。细胞学检查显示,两处取样区域均存在数量相近的巨噬细胞和非变性中性粒细胞,没有发现微生物或肿瘤细胞。
心包/胸膜液混合物被送去进行需氧/厌氧细菌和真菌培养以及猫冠状病毒(FCoV)及巴尔通体PCR检测。结果发现外周血和胸膜/心包积液巴尔通体PCR检测结果均为阳性。测序、分析和比对后发现,两个样本与汉氏巴尔通体100%吻合。培养物中未发现生长,FCoV实时PCR结果为阴性。
03 治疗
住院期间使用了马波沙星(5 mg/kg SC q24h)和阿莫西林-克拉维酸(62.5 mg/只 IV q12h)以及跳蚤治疗(氟虫腈喷雾剂、吡虫啉和莫西菌素点涂剂)。
04 预后
几天后,情况有所好转,发烧也退了。随访的放射线检查和超声心动图检查均未发现渗出。出院时服用了马波沙星(5 mg/kg PO q24h)和阿莫西林-克拉维酸(62.5 mg/只 PO q12h)。培养结果呈阴性后,阿莫西林-克拉维酸停用,但继续使用了马波沙星。
1个月后,贫血症状缓解,也没有渗出。但在接受马波沙星单药治疗时,再次出现血液巴尔通体PCR阳性。于是停用了马波沙星,开始使用多西环素(5 mg/kg PO q12h)。
使用多西环素6周后,血液巴尔通体PCR呈阴性,停止了多西环素治疗。
3年后,仍然健康,超声心动图复查显示没有心包积液或胸腔积液。
05 讨论
巴尔通体病(Bartonellosis)是一种由巴尔通体(Bartonella)引起的病媒传播人畜共患病[1]。在哺乳动物(包括猫、狗和人类)中,巴尔通体感染的记录十分详尽,并且与各种临床表现和疾病严重程度有关[1]。
猫是汉氏巴尔通体(Bartonella henselae)的主要宿主,而汉氏巴尔通体是人类猫抓病的病原体[1-3]。在人类和犬患者的腔隙性渗出物中,汉氏巴尔通体的分离频率相对较高,有时很难确定它是病原体还是机会性病原体[1-4]。
据报道,猫感染巴尔通体后出现的临床症状、病变和实验室异常包括发烧、淋巴结肿大、贫血、嗜酸性粒细胞增多、高球蛋白血症、血小板减少、膈肌炎、心内膜炎、脓毒血症性心肌炎、心内膜纤维化综合征、轻度神经症状、葡萄膜炎、结膜炎、角膜炎、角膜溃疡、关节炎和骨髓炎[6]。然而,在没有并发心衰的猫中,还未见过与巴尔通体感染相关的胸腔和/或心包积液的报道[1,6,8]。
本患者心包积液的一种可能解释是由巴尔通体病引起的感染性心包炎。猫细菌性心包炎很少见,一项对146只猫的心包积液进行的回顾性研究发现,没有化脓性心包炎病例[9]。另一项对83只患有心包积液的猫进行的研究发现,肥厚型心肌病、肿瘤和全身感染是主要原因,而由巴尔通体以外的细菌引起的猫细菌性心包炎的病例报告也很少[8,10-13]。这就提出了一个问题:巴尔通体是否会产生类似的临床表现?
猫胸腔积液最常见的原因包括充血性心衰、猫传腹、肿瘤、脓胸或乳糜胸[14]。本患者有心包填塞,这可能是胸腔积液的原因。另一种可能是血源性传播导致的胸膜炎,或者是汉氏巴尔通体引起的内皮损伤导致的血管炎[15-22]。
本患者的渗出物被归类为富含蛋白质的渗出物。渗出物通常表示细菌感染引起的炎症反应,但这并不总是适用于巴尔通体感染。巴尔通体的脂多糖具有抗炎特性,而研究表明巴尔通体的亚种可导致免疫抑制[21,24,25]。
总之,本病例强调了将巴尔通体病作为患有蛋白渗出液、中性-巨噬细胞炎症和发烧猫的鉴别诊断的重要性。临床症状很可能与汉氏巴尔通体感染有关,因为没有发现其他病因,而且患者对治疗反应积极。要更好地了解这种病原体对健康、非免疫力低下的猫的影响,并确定其发病率的特征,还需要进一步的研究和病例分析。
文献来源:Torrano Guillamón A, Juarez Sarrión C, Álvarez Fernández A, Solano-Gallego L, González Villajos C, Arenas Bermejo C, Castro López J. Pleural and pericardial effusion associated with Bartonella henselae infection in a feline patient. JFMS Open Rep. 2025 Feb 27;11(1):20551169251313617.
参考文献
1. Álvarez-Fernández A, Breitschwerdt E, Solano-Gallego L. Bartonella infections in cats and dogs including zoonotic aspects. Parasites Vectors 2018; 11: 624.
2. Bergh K, Bevanger L, Hanssen I, et al. Low prevalence of Bartonella henselae infections in Norwegian domestic and feral cats. APMIS 2002; 110: 309–314.
3. Solano-Gallego L, Hegarty B, Espada Y, et al. Serological and molecular evidence of exposure to arthropod-borne organisms in cats from northeastern Spain. Vet Microbiol 2006; 118: 274–277.
4. Kordick D, Brown T, Shin K, et al. Clinical and pathologic evaluation of chronic Bartonella henselae or Bartonella clarridgeiae infection in cats. J Clin Microbiol 1999; 37: 1536–1547.
5. Álvarez-Fernández A, Maggi R, Martín-Valls GE, et al. Prospective serological and molecular cross-sectional study focusing on Bartonella and other blood-borne organisms in cats from Catalonia (Spain). Parasit Vectors 2022; 15: 6.
6. Taber R, Pankowski A, Ludwig AL, et al. Bartonellosis in dogs and cats, an update. Vet Clin North Am Small Anim Pract 2022; 52: 1163–1192.
7. Bradbury CA, Lappin MR. Evaluation of topical application of 10% imidacloprid-1% moxidectin to prevent Bartonella henselae transmission from cat fleas. J Am Vet Med Assoc 2010; 236: 869–873.
8. Davidson BJ, Paling AC, Lahmers SL, et al. Disease association and clinical assessment of feline pericardial effusion. J Am Anim Hosp Assoc 2008; 44: 5–9.
9. Hall DJ, Shofer F, Meier CK, et al. Pericardial effusion in cats: a retrospective study of clinical findings and outcome in 146 cats. J Vet Intern Med 2007; 21: 1002–1007.
10. LeBlanc N, Scollan KF. Bacterial pericarditis in a cat. JFMS Open Rep 2015; 1.
11. Lobetti RG. Anaerobic bacterial pericardial effusion in a cat. J S Afr Vet Assoc 2007; 78: 175–177.
12. Brook I. Pericarditis caused by anaerobic bacteria. Int J Antimicrob Agents 2009; 33: 297–300.
13. Majoy SB, Sharp CR, Dickinson AE, et al. Septic pericarditis in a cat with pyometra. J Vet Emerg Crit Care (San Antonio) 2013; 23: 68–76.
14. König A, Hartmann K, Mueller R, et al. Retrospective analysis of pleural effusion in cats. J Feline Med Surg 2018; 21: 1102–1110.
15. Levy P, Fournier P, Carta M, et al. Pericardial effusion in a homeless man due to Bartonella quintana. J Clin Microbiol 2003; 41: 5291–5293.
16. Takeda N, Ishiwada N, Fukasawa C, et al. Pediatric pneumonia, pleural effusion, and pericarditis following cat scratch disease and serological cross-reactions among Bartonella henselae and Rickettsia japonica determined by indirect fluorescence antibodies [article in Japanese]. Kansenshogaku Zasshi 2007; 81: 206–209.
17. Kimura S, Hasegawa S, Yanagihara M, et al. Cat-scratch disease with severe pleuritis in a 6-year-old girl. Pediatr Int 2015; 57: 501–503.
18. Sodini C, Zani EM, Pecora F, et al. A case of atypical Bartonellosis in a 4-year-old immunocompetent child. Microorganisms 2021; 9.
19. Karanyi K. Fever, back pain and pleural effusion in a four-year-old boy. Pediatr Infect Dis J 1994; 13: 657–672.
20. Weeden AL, Cherry NA, Breitschwerdt EB, et al. Bartonella henselae in canine cavitary effusions: prevalence, identification, and clinical associations. Vet Clin Pathol 2017; 46: 326–330.
21. Cherry N, Diniz P, Maggi R, et al. Isolation or molecular detection of Bartonella henselae and Bartonella vinsonii subsp.berkhoffii from dogs with idiopathic cavitary effusions. J Vet Intern Med 2009; 23: 186–189.
22. Duncan A, Marr H, Birkenheuer A, et al. Bartonella DNA in the blood and lymph nodes of golden retrievers with lymphoma and in healthy controls. J Vet Intern Med 2008; 22: 89–95.
23. Tabar M-D, Movilla R, Serrano L, et al. PCR evaluation of selected vector-borne pathogens in dogs with pericardial effusion. J Small Anim Pract 2018; 59: 248–252.
24. Popa C, Abdollahi-Roodsaz S, Joosten LAB, et al. Bartonella quintana lipopolysaccharide is a natural antagonist of Toll-like receptor 4. Infect Immununity 2007; 75: 4831–4837.
25. Pappalardo BL, Brown TT, Tompkins M, et al. Immunopathology of Bartonella vinsonii (berkhoffii) in experimentally infected dogs. Vet Immunol Immunopathol 2001; 83: 125–147.