| 品种:混种猫 | |
| 年龄:7个月 | |
| 性别:雄 | |
| 诊断:先天性甲减 | |
01 主诉及病史
因生长缓慢、乳牙脱落延迟和前肢变形性骨质营养不良等生长障碍而被转诊。
02 检查
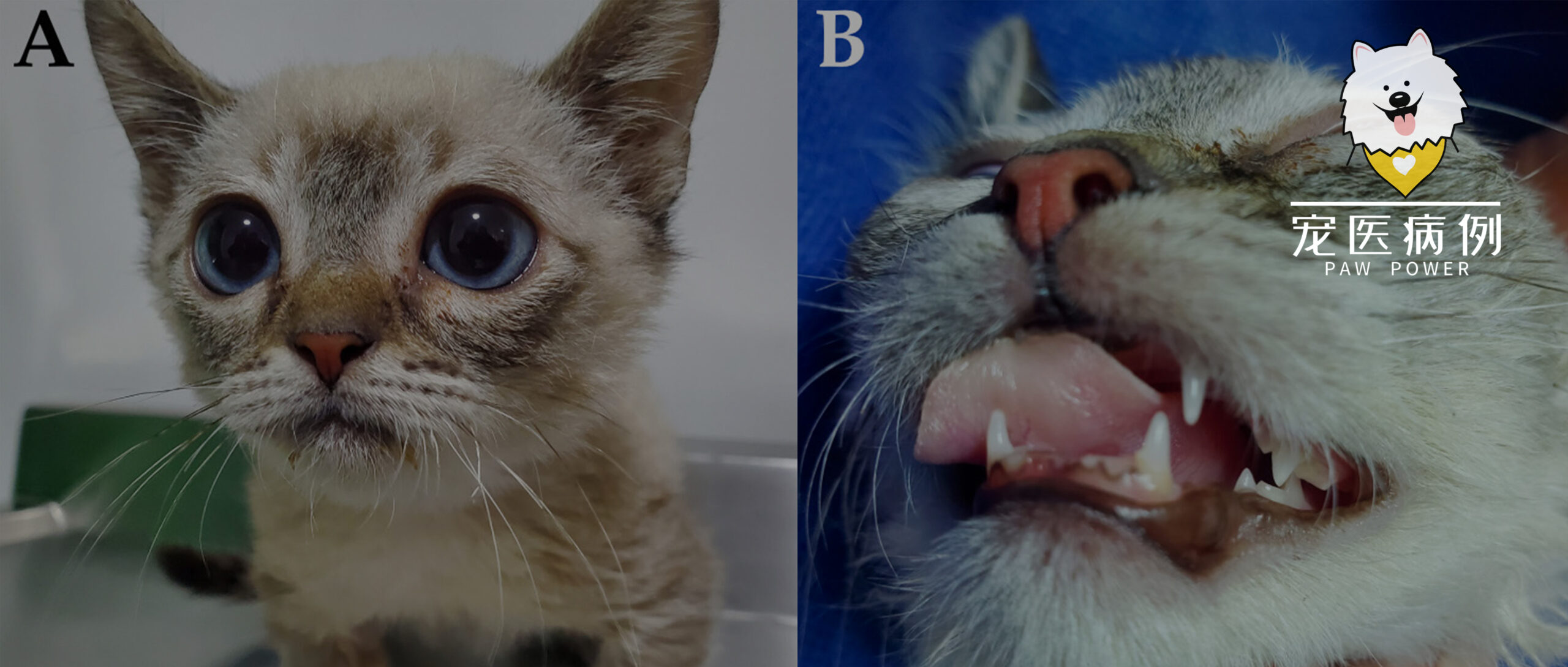
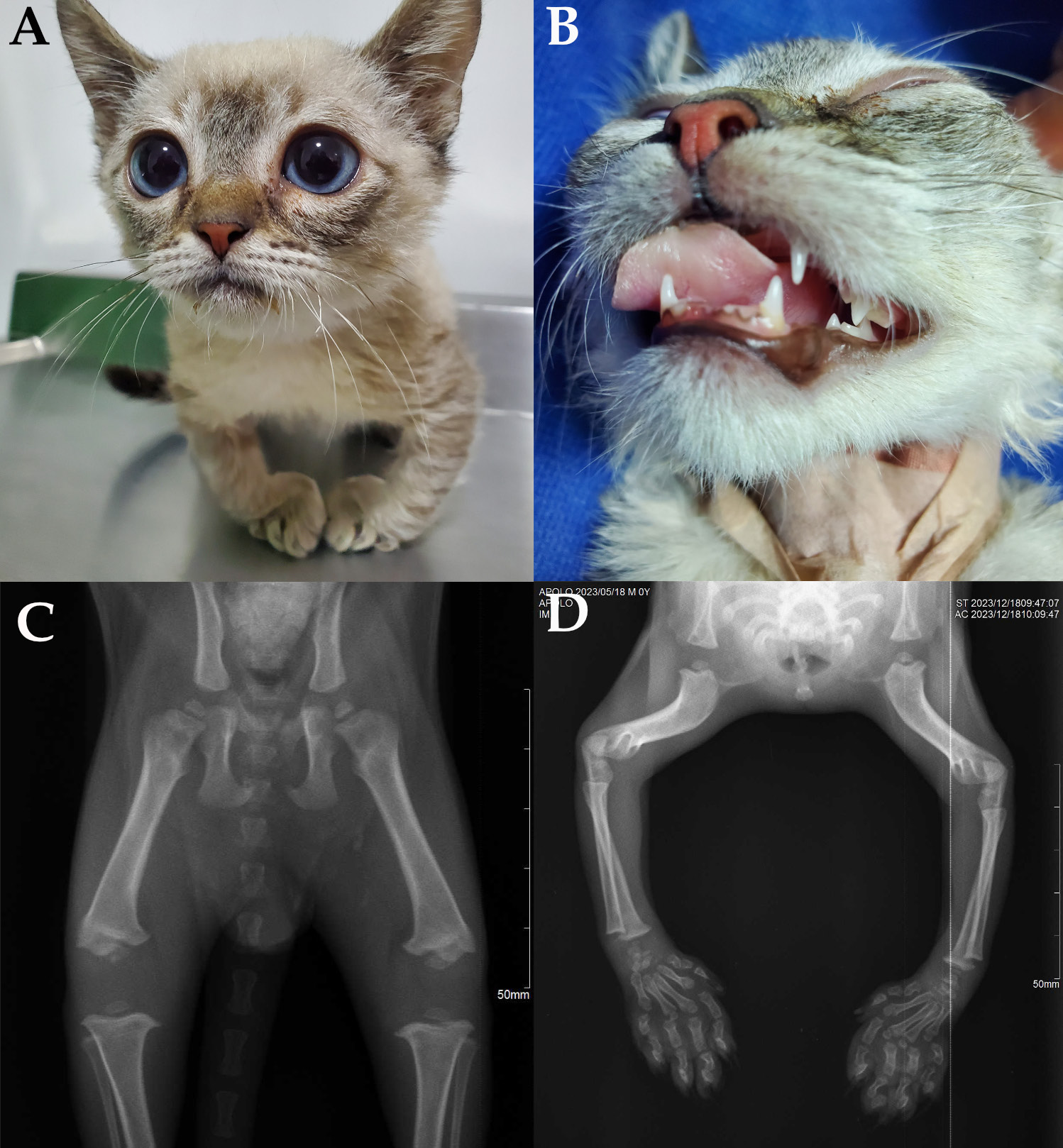
患者外观如下图,表现为发育异常、出生后生长速度下降、头宽、眼睛大、前肢骨营养不良(下图A)、乳牙脱落延迟和门牙萌出缺失(下图B)。髋关节的放射线检查显示髋关节发育不良,骨盆闭合不全,膝关节形成不全(下图C),肩胛骨-肱骨关节、肘关节和腕骨-桡骨-尺骨关节的骨骺发育不良(下图D)。
血红蛋白浓度8.3 g/L [9.3-15.3],红细胞压积26.3% [28%-49%],血尿素氮55.1 mg/dL [4.5-23.5],平均体温37°C。IGF-1、T4和TSH的测量结果分别为38 μg/dl [200-800]、0.5 μg/dl [0.8-4.7]和0.82 UI/ml [0.00-0.20],被诊断为甲状腺功能减退症。
03 治疗
开始使用左旋甲状腺素20 μg/kg进行治疗,每24小时一次。
由于便秘问题,接受了两次手术,以清除结肠中积聚的粪便,但效果不佳。
04 预后
第二次肠切开术一周后,出现严重的并发症,并死亡。尸检结果显示,患者存在巨结肠、双侧甲状腺叶肿大(下图A)和左心室肥大(下图B)。

↑ 双侧甲状腺肿大(A)。左心室肥大(B)。
组织病理学检查显示,甲状腺滤泡发育不良,胶体物质稀少(下图C),滤泡旁细胞数量减少,结缔组织疏松,滤泡细胞中存在细胞质颗粒(下图D)。
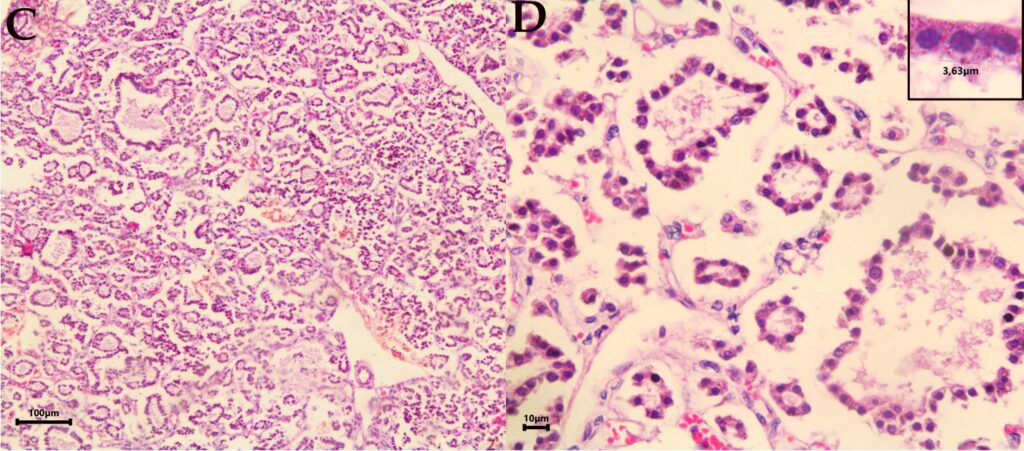
↑ 观察到大小不一的甲状腺滤泡和浓度极低的胶质(C)。甲状腺滤泡发育不良,周围有疏松的结缔组织和少量滤泡旁细胞,甲状腺细胞(方框)中有明显的胞浆内颗粒(D)。
进行了基因检测,对TPO基因的3个区域进行了PCR扩增,这3个区域含有之前在猫和狗中报道过的单核苷酸多态性。序列比较显示,核苷酸12,542处存在变异(A > G)(下图A)。还发现了先前在其他猫身上描述过的变异(下图B)。最后,对对照组狗身上描述的变异位点片段进行分析,对照组患者在核苷酸 30713(G>C)上存在变异,而本患者在该位置上存在基因多态性(下图C)。

05 讨论
先天性甲状腺功能减退症(Congenital hypothyroidism,CH)是家养动物中一种罕见的、诊断率低的内分泌疾病,其特征是甲状腺发育不良或激素生成障碍[1,2]。
临床症状与甲状腺激素生理功能失调密切相关,与肌肉和大脑发育不良、能量平衡改变、发育异常(如不成比例的侏儒症)有关、 头大、脸扁、颈部、身体和四肢较小、牙齿萌出延迟、骺发育不良、趾骨闭合延迟等发育异常,以及出现可触及的双侧移动性甲状腺肿、心动过缓、体温过低、舌肿胀和肌张力减弱等症状[2-4]。在人类中,早产、低促甲状腺激素(TSH)和妊娠期甲状腺素(T4)暴露往往是导致新生儿CH的原因之一[5]。不过,这种情况在伴侣动物中还没有出现过。
在患有CH的人类中,一些基因的变异与发育不良和激素生成障碍有关,后者以隐性方式遗传[2],与TPO(甲状腺过氧化物酶)、DUOX2、DUOXA2、SLC26A4、SLC5A5、TG和IYD等基因的突变有关[1,2,4]。在患有CH的狗和猫中,已发现其中一些基因发生了突变,从而影响了相应蛋白质的合成和功能[1,2]。
CH的诊断依据是临床症状以及血液中T4和TSH浓度的测量结果;此外,闪烁照相法也可用于区分发育不良和激素生成障碍[2]。由于该病罕见且诊断困难,许多患者在出生时或出生后早期发育阶段死亡[2]。分子检测很少用于家畜CH的诊断,而且几乎只用于研究,但分子检测有助于了解CH的发病机制[6]。
通过对犬TPO基因组序列的分析,确定了Fyfe等人[7]和Major等人[8]所描述的突变位点,并通过随后的犬猫序列比对,发现了本病例猫基因组序列中的保守区,从而预测了猫基因组序列中可能出现的突变。
对本病例猫的TPO不同区域进行的测序分析表明,该变异从A>G转变而来,即编码Gln的密码子变为编码Arg的密码子。值得注意的是,该变异与Fyfe等人[7]在玩具猎狐犬身上发现的变异处于同源位置,Fyfe等人报告说,在患有CH的狗身上发现了C>T的转变,产生了过早终止密码子,导致无功能截短蛋白的翻译,此外,在健康患者身上也发现了相同变异的多态性。
虽然临床表现和临床辅助检查可以诊断甲状腺功能减退症,但分子检测有助于明确先天性内分泌病,因此,分子技术是了解CH的一种工具。在某些犬种中,用于检测TPO突变的分子检测方法已经标准化[7]。此外,在一些国家,人类新生儿CH诊断测试的使用也很普遍[4],从而实现了早期检测和治疗。
总之,本报告首次在一只患有CH的猫体内发现了TPO基因的三种变异,其中包括可能与疾病发展有关的多态性。尽管如此,要了解CH,还需要研究可能在该病的起源和临床表现中起作用的多个基因。分子特征描述是准确快速诊断的重要工具。
文献来源:Gallego-Munevar C, Carrillo-Godoy N, Rondón-Barragán IS. Molecular detection of a novel mutation in the TPO gene associated with congenital hypothyroidism in a cat: Case report. J Adv Vet Anim Res. 2024 Dec 29;11(4):1030-1036.
参考文献
[1].Soler Arias EA, Castillo VA, Garcia JD, Fyfe JC. Congenital dyshormonogenic hypothyroidism with goiter caused by a sodium/iodide symporter (SLC5A5) mutation in a family of Shih-Tzu dogs. Domest Anim Endocrinol. 2018;65:1–8.
[2].Van Poucke M, Van Renterghem E, Peterson ME, van den Berg MF, Stock E, Peelman LJ, et al. Association of recessive c.430G>A (p.(Gly144Arg)) thyroid peroxidase variant with primary congenital hypothyroidism in cats. J Vet Intern Med. 2022;36(5):1597–606.
[3].Iturriaga MP, Cocio JA, Barrs VR. Cluster of cases of congenital feline goitrous hypothyroidism in a single hospital. J Small Anim Pract. 2020;61(11):696–703.
[4].Naqvi SF, Yıldız-Bölükbaşı E, Afzal M, Nalbant G, Mumtaz S, Tolun A, et al. Homozygous mutations in thyroid peroxidase (TPO) in hypothyroidism with intellectual disability, developmental delay, and hearing and ocular anomalies in two families: severe manifestation of untreated TPO-deficiency poses a diagnostic dilemma. Yale J Biol Med. 2023;96(3):347–65.
[5].Eng L, Lam L. Thyroid function during the fetal and neonatal periods. Neoreviews. 2020;21(1):e30–6.
[6].Begum MN, Mahtarin R, Islam MT, Antora NJ, Sarker SK, Sultana N, et al. High-resolution melt curve analysis: an approach for variant detection in the TPO gene of congenital hypothyroid patients in Bangladesh. PLoS One. 2024;19(4):e0293570.
[7].Fyfe JC, Kampschmidt K, Dang V, Poteet BA, He Q, Lowrie C, et al. Congenital hypothyroidism with goiter in toy fox terriers. J Vet Intern Med. 2003;17(1):50–7.