一般情况
| 品种 | 短毛猫 |
| 年龄 | 4.5岁 |
| 性别 | 雄 |
| 是否绝育 | 是 |
| 诊断 | 禽流感 |
01 主诉及病史
因嗜睡、厌食和持续发热4天被转诊。
该猫平时完全室内饲养,但在就诊前约1周曾有一次短暂无人看管的逃出家门。逃跑范围仅限于后院,约10分钟内即被找回。期间主人见其啃咬一盆朱顶红属盆栽,但未观察到明显吞食。既往无其他外出史、毒素或野生动物接触史,也未喂食生肉、生肉零食或生乳,所有疫苗(包括狂犬疫苗)均按时接种。
转诊前2天,初级兽医体格检查见黏膜苍白、脱水5-8%、呼吸急促(60次/分)、心动过速(150次/分)及高热(39.9°C)。肝实质细胞和胰腺酶活性显著升高,伴高血糖、低钙血症、低磷血症、白细胞减少及血小板减少;但未做血涂片复核。尿比重>1.040,轻度蛋白尿、糖尿,白细胞酯酶阳性,轻度脓尿。腹部超声仅见胆囊壁增厚,无胰腺炎或胃肠炎征象。猫白血病病毒、猫免疫缺陷病毒及心丝虫均阴性。
初诊治疗:乳酸林格液(4.5 ml/kg/h)、枸橼酸马罗匹坦(1 mg/kg SC一次)、阿莫西林-克拉维酸(11 mg/kg PO q12h)及罗贝考昔(1.05 mg/kg PO q24h)。2天后病情恶化,遂转诊。
02 检查
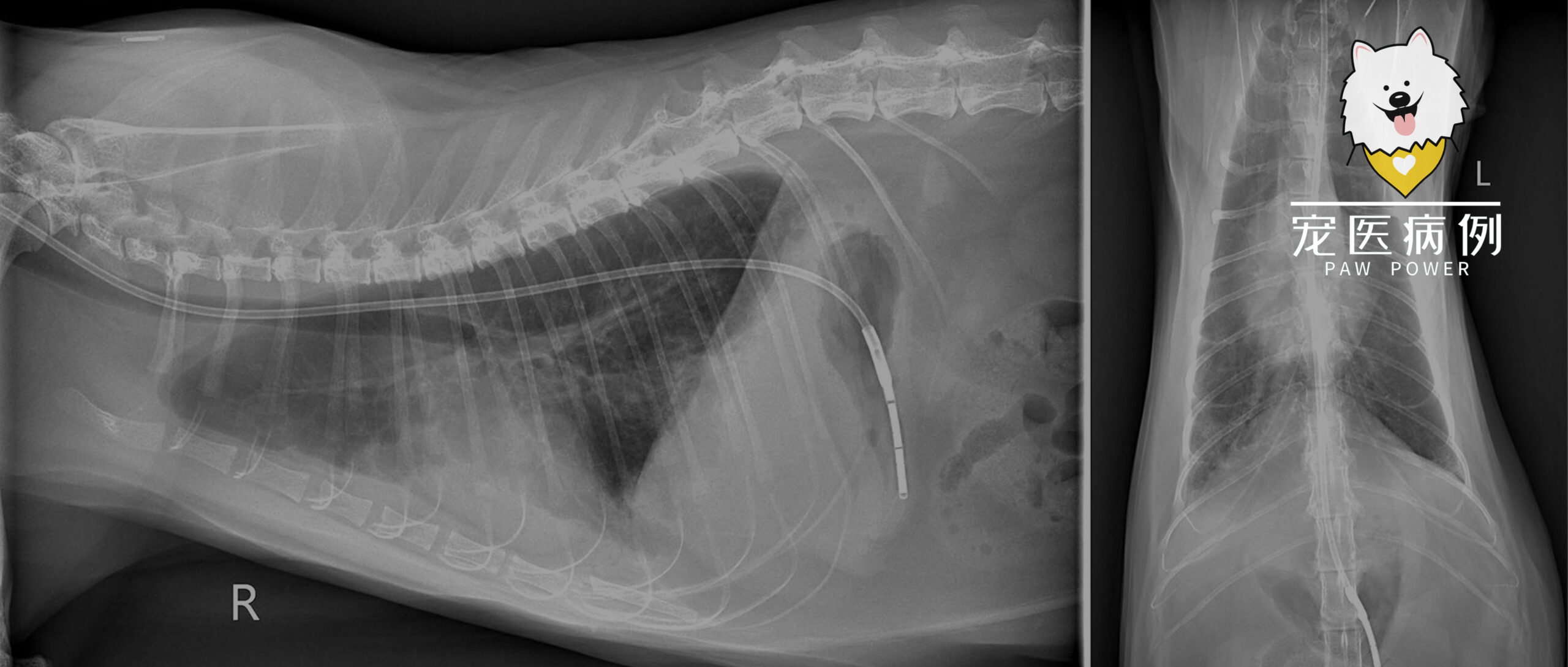
体重5.9 kg。精神沉郁,呼吸急促(100次/分),高热(41.2°C)。胸部X线呈混合性肺征,间质、支气管及肺泡均受累,后叶最严重(图1)。轻度胸腔积液与心脏增大,提示心肺疾病。
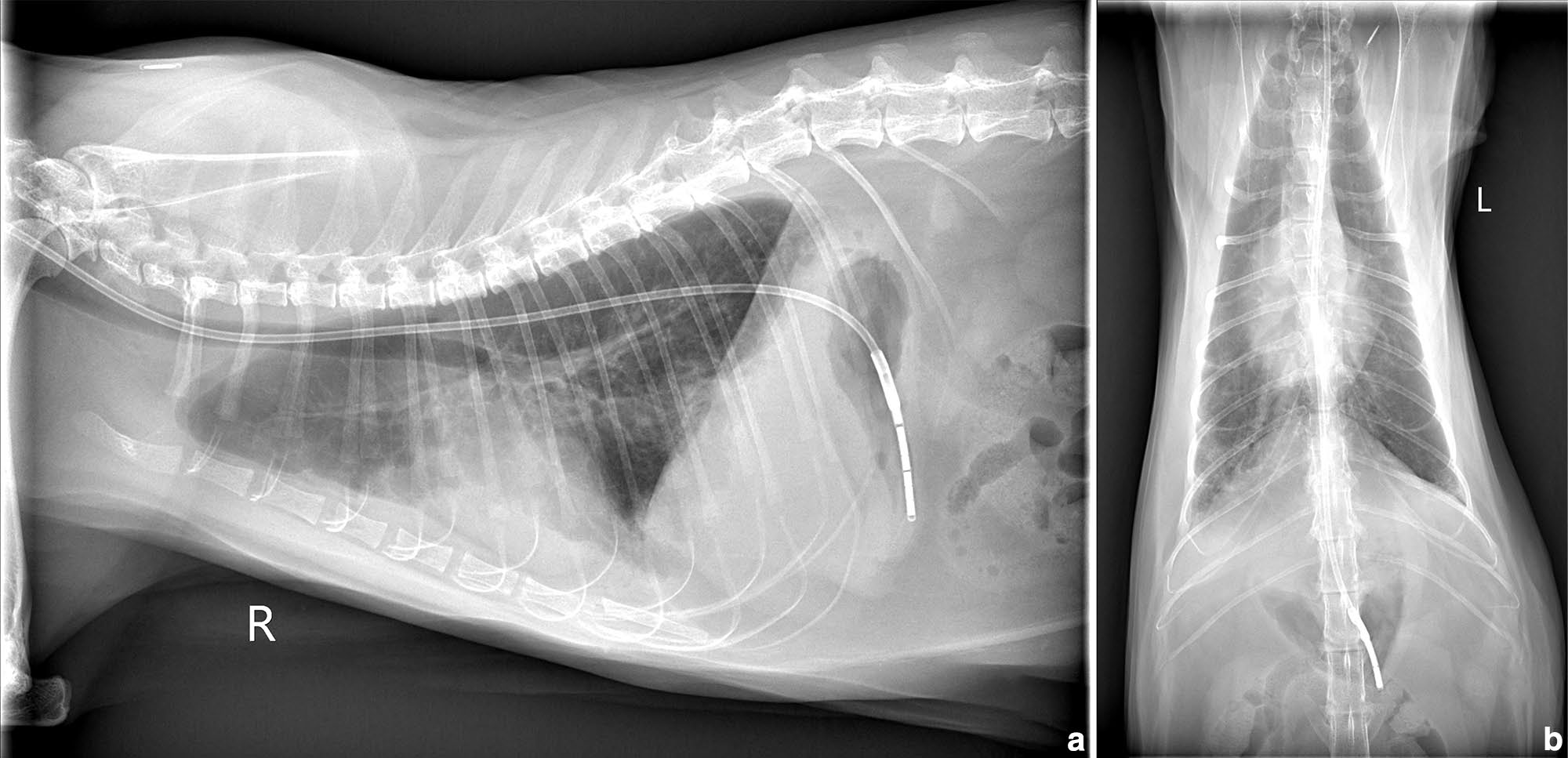
图1. 胸部X线片(a)侧位:弥漫混合性肺征,间质、支气管及肺泡病变以后叶最显著,伴轻度胸腔积液及中度心脏影增大。(b)背腹位:更清楚显示胸腔积液及肺、心细节。
猫SNAP proBNP检测:血清(未稀释)阴性,胸腔积液1:1稀释后阳性。胸腔积液细胞学示高蛋白改性漏出液,主要为非变性中性粒细胞、空泡化巨噬细胞及淋巴细胞。
复查血象:全低蛋白血症、肝损伤、横纹肌溶解、高胆红素血症、电解质紊乱、轻度高血糖,白细胞及血小板减少加重,涂片见聚集。
尿沉渣:移行/肾小管上皮细胞脱落(6–10/hpf)、颗粒管型(0–1/lpf)、糖尿(3+)、胆红素尿(3+)、脓尿(4–8 WBC/hpf)。
血清学传染病检测:巴尔通体、血支原体、埃里希体/无形体/新立克次体/沃尔巴克体PCR及弓形虫IgM/IgG ELISA均阴性。
03 治疗
支持治疗包括吸氧(60%)、静脉乳酸林格液(2 ml/kg/h)、氯化钾补液(0.5 mEq/kg/h,持续2 h)、马罗匹坦(1 mg/kg IV q24h)、昂丹司琼(0.5 mg/kg IV q8h)及氨苄西林-舒巴坦(30 mg/kg IV q8h)。
6小时后复查血象:钠、钾、氯改善,但低钙血症持续,高血糖及高乳酸血症加重。猫出现进行性神经症状:共济失调、癫痫、意识迟钝,伴呼吸窘迫恶化。
因预后极差,主人选择安乐死,并同意尸检。
04 尸检
双肺弥漫坚实、充气不良,各叶暗红至红褐色,可见气道为中心的结节状病灶,切面溢出黏液血性液体,伴周围实质放射状线性出血。肝脏均匀赭色,边缘钝圆,表面呈明显网状;散在、融合、边界不清的樱桃红斑,正常小叶结构消失。
心脏重25.2 g,右室壁3 mm、室间隔13 mm、左室壁14 mm,符合肥厚型心肌病。胸腔(30 ml)及腹腔(15 ml)均有少量浆血性积液。幽门括约肌附近见1 ×0.3 cm线状慢性活动性胃溃疡,边缘为坚实纤维组织;小肠内见中等量樱桃红血液,至空肠-回肠交界处转为黑色液体。
组织学:脑、肺、肝、淋巴结及胰腺均见严重坏死性病变。脑灰质为主,呈坏死性、中性粒细胞性脑膜脑炎,伴神经元噬食、星形胶质细胞增生及微血管肥厚(图2)。

图2. 光学显微照片(a)受累神经毡区域性稀疏,胶质细胞增多,神经元固缩、嗜酸增强,核淡染或固缩;小胶质细胞及偶见中性粒细胞环绕变性坏死神经元及其碎片。(b)血管炎症,内弹力板节段断裂,管壁被亮嗜酸性无结构物质(纤维素样坏死)充填,内混细胞碎片及少量混合炎细胞。
肺示纤维蛋白坏死性支气管间质性肺炎(图3)。肝内病灶为随机分布的多发凝固-溶解性肝细胞坏死;外分泌胰腺及多处淋巴结亦见类似坏死。左室心肌排列紊乱,证实肥厚型心肌病。其余组织学改变轻微,无临床意义。
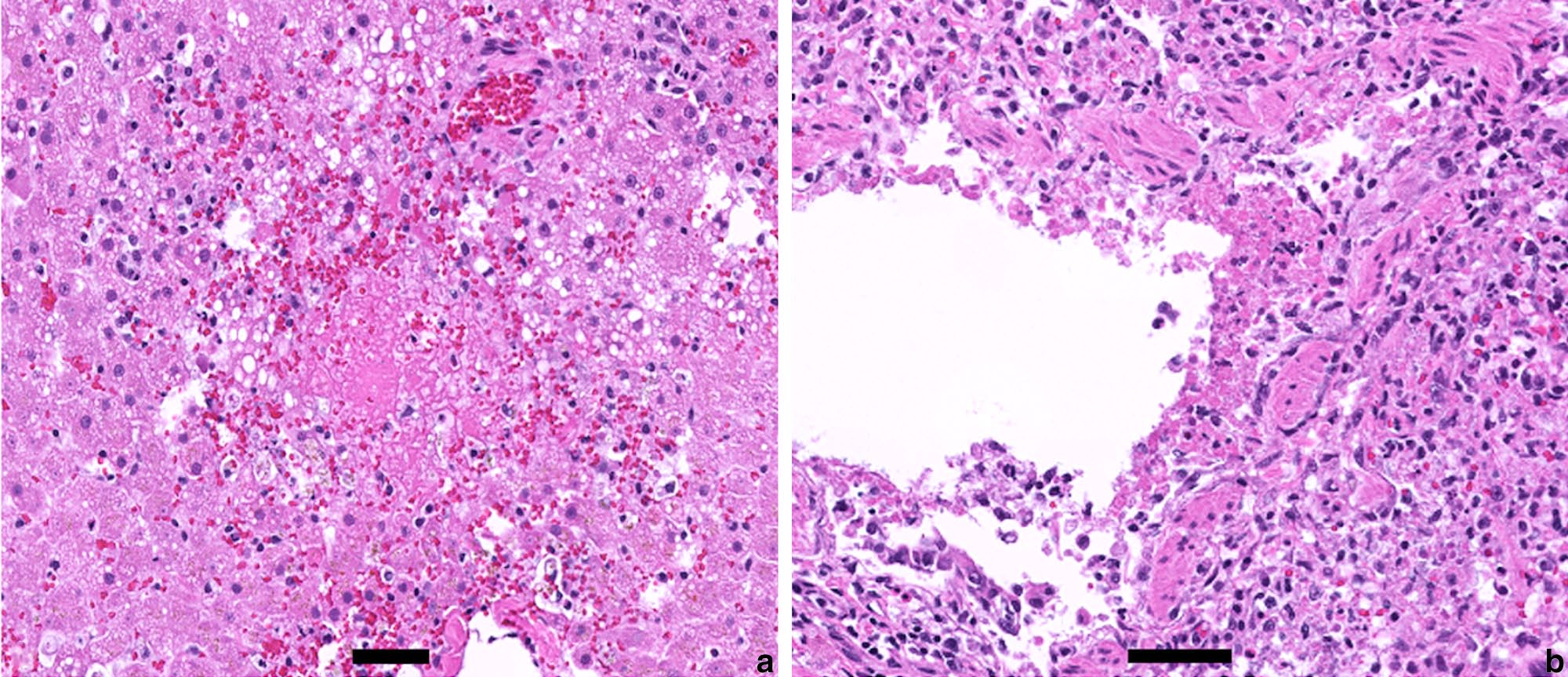
图3. 光学显微照片(a)肝实质坏死,肝细胞消失,代之以大量外渗红细胞、纤维素及细胞与核碎裂碎片。(b)小支气管节段性坏死,上皮细胞脱落,表面附着纤维素丝。
肺和脑组织的实时RT-PCR检测确认存在H5亚型禽流感病毒及甲型流感病毒。由于未建立标准曲线,未进行绝对定量,但循环阈值(Ct)较低,提示病毒载量高(脑:H5 Ct 12.84,甲流Ct 10.68;肺:H5 Ct 17.55,甲流Ct 14.92)。后续由国家兽医服务实验室测序确认病毒为2.3.4.4b-B3.13分支,与北美野生动物和家禽中流行的毒株一致。狂犬病间接荧光抗体检测阴性;肺组织猫杯状病毒、疱疹病毒-1及衣原体PCR均阴性。脑组织未培养出细菌;组织切片镜检亦未见其他病原体。
05 讨论
高致病性禽流感(HPAI)H5N1 属甲型流感病毒,野生水禽为自然储存宿主。2022年再次传入北美后,已跨越物种屏障感染家畜与多种野生哺乳动物。
猫因捕食天性、生食习惯及中枢神经系统富含α-2,3-唾液酸受体,对H5N1高度易感,临床可从隐性感染骤变为暴发性多系统炎症,死亡率逾80%。
病毒主要经摄入染疫禽肉、污染乳或环境媒介进入体内,沿迷走神经上行,引发坏死性脑炎与重症支气管间质性肺炎,并继发肝、胰、淋巴等多器官播散。
人兽共患风险随病毒载量升高而增大,尤其当家庭内同时存在人流感毒株时,理论上有发生基因重配、获得人际传播能力的潜在可能。
本例家养短毛猫,平日完全室内饲养,仅于发病前一周短暂逃出后院10 min,无明确禽类接触史,仍感染clade 2.3.4.4b-B3.13亚型H5N1。RT-PCR显示肺与脑组织病毒载量极高,说明少量环境暴露即可引发严重感染,间接提示病毒在局部野生小型哺乳动物或污染物中已呈高负荷循环。
患猫4天内迅速出现高热、厌食、呼吸窘迫及神经症状,实验室特征为白细胞与血小板锐减、肝胰酶飙升、肌酸激酶>80 000 IU/l,伴低钙、低钠、乳酸性酸中毒,与既往报道的“细胞因子风暴”表现相符。
影像及尸检证实弥漫性支气管间质性肺炎、出血性肝坏死、坏死性胰炎及灰质为主脑膜脑炎,同时合并肥厚型心肌病,可能因低氧与代谢紊乱加重循环负荷,加速死亡。
治疗上虽给予高流量氧、静脉补液、广谱抗生素及镇吐、解热等积极支持,仍未能逆转多器官衰竭,提示一旦出现神经症状,抗病毒窗口极短。
总之,本病例首次在几乎完全室内饲养的宠物猫身上证实H5N1可经微量环境途径感染并导致高载量神经嗜性病变,扩展了人们对非典型暴露风险的认识。结果强烈提示:
- 即使缺乏生食或禽类接触史,室内猫出现急性高热-神经-呼吸三联症时,应将HPAI纳入鉴别诊断,及早进行呼吸道与脑组织RT-PCR检测;
- 病毒2.3.4.4b分支已牢固建立跨物种传播链,野生小型哺乳动物可能充当“桥梁宿主”,应加强对其感染监测及垃圾、尸体无害化处理;
- 家庭同时出现宠物与人流感样症状时,必须同步采样、测序,以排除病毒重配与新型毒株诞生;
- 鉴于高致死率,研发动物专用神经氨酸酶抑制剂及疫苗、建立猫群应急免疫屏障已迫在眉睫;
- 兽医、公共卫生与野生动物管理部门应共享数据,实施“同一健康”联防联控,方能降低H5N1在人类和城市动物中的暴发风险。
文献来源:Granger KL Jr, Gross C, Frank C, Lappin MR. Multisystemic manifestations of highly pathogenic avian influenza (H5N1) in a young domestic shorthair cat. JFMS Open Rep. 2025 Nov 11;11(2):20551169251376559.