一般情况
| 品种 | 波斯猫 |
| 年龄 | 14岁 |
| 性别 | 雌 |
| 是否绝育 | 是 |
| 诊断 | 耵聍腺腺癌 |
01 主诉及病史
因左外耳道肿物被转诊。
此前在当地动物医院经切取活检诊断为耵聍腺腺癌,正接受托西尼布(2.5 mg/kg,口服)治疗。尽管用了药,但左外耳道瘙痒加重且肿物持续增大。
02 检查
体重3.09 kg。整体状态稳定,食欲、排尿、排便正常;检查时精神机敏,无全身症状。体况评分3/9,皮肤弹性略差提示轻度脱水。
左外耳道内可见中等量褐色蜡样分泌物及坚硬不规则肿物,周围腮腺区轻度肿胀;左眼睑反射消失,提示面神经功能障碍,其余脑神经反射正常。下颌及肩前淋巴结未触及肿大,无前庭或步态异常,耳部操作仅引起轻度疼痛,猫耐受良好。
胸片未见肺转移;血液学及生化指标均在参考范围内。为评估肿瘤范围并制定放疗计划,全麻下行增强CT及MRI检查。CT显示左垂直耳道被巨大软组织肿物完全阻塞,并侵及邻近腮腺和下颌区域(图1)。增强扫描肿物呈显著均匀强化,左侧咀嚼肌及下颌腺亦呈相似强化且边界不清,提示肿瘤直接侵犯。
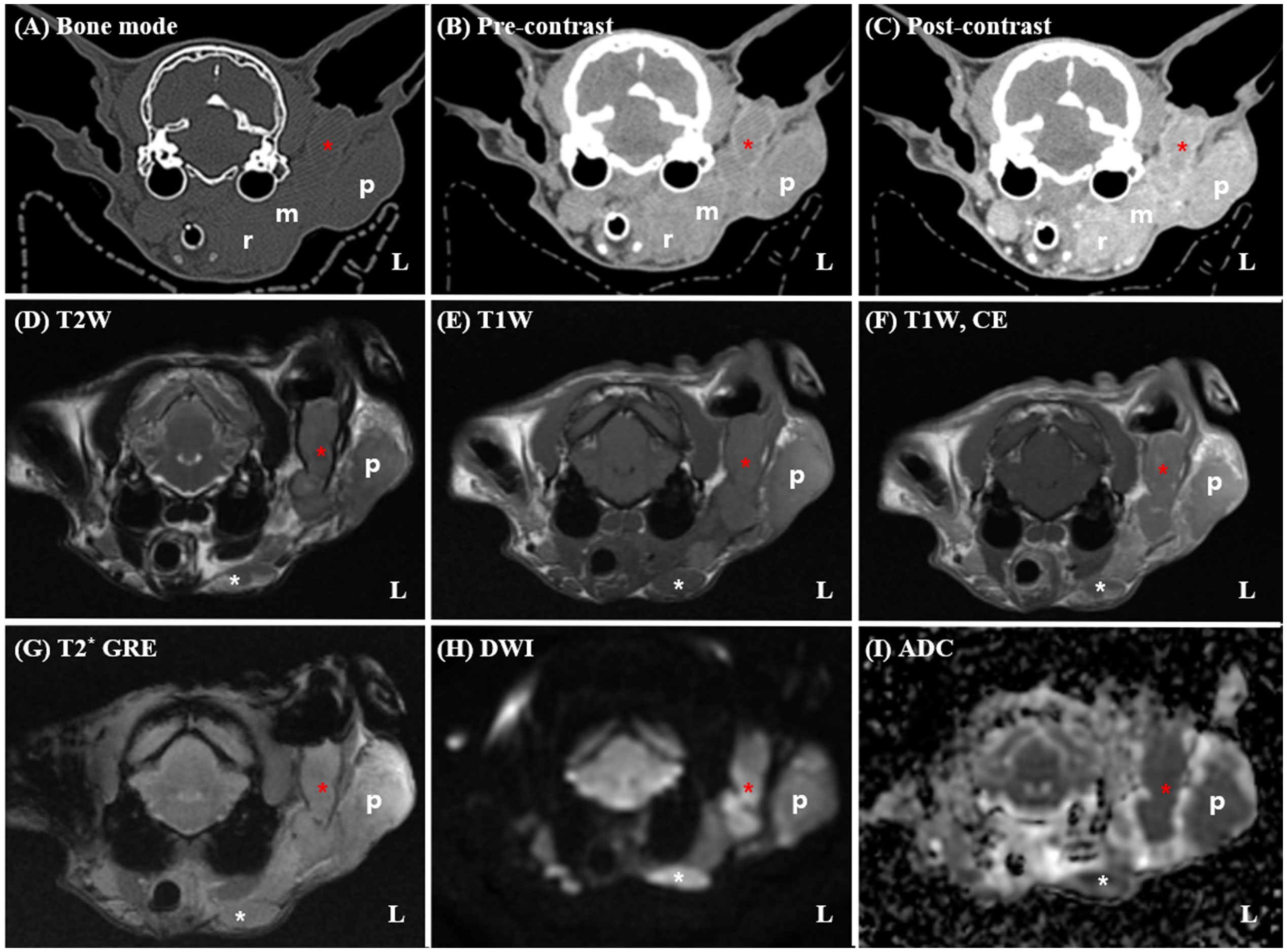
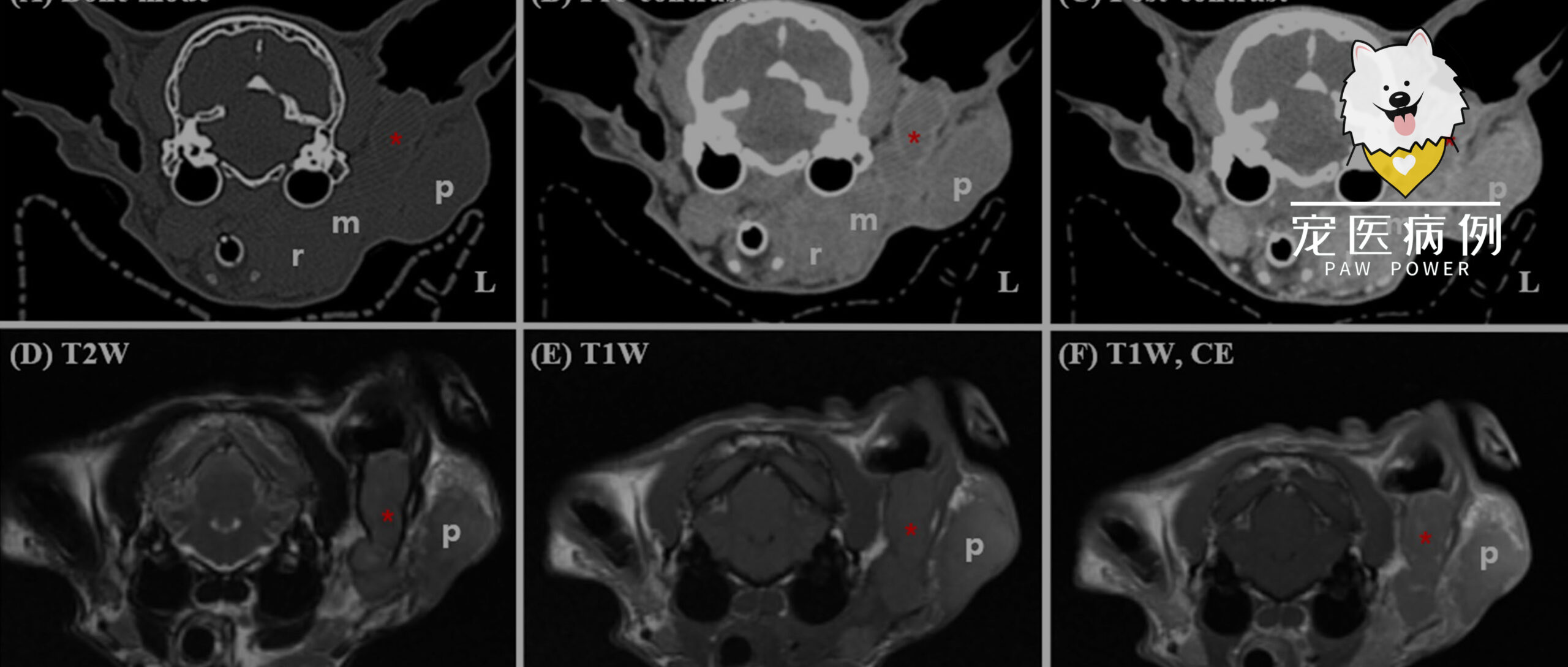
图1. 放疗前CT(A–C)与MRI(D–I)影像。CT及MRI示巨大软组织肿块(红色星号)占据左侧垂直外耳道,并延伸至邻近腮腺(p)及下颌区域。增强CT及T1加权MRI(C、F)显示肿块呈显著均匀强化,其与周围结构(咬肌及下颌腺,m)分界不清,提示直接侵犯。同侧下颌(白色星号)及内侧咽后淋巴结(r)明显增大。左侧外侧咽后淋巴结与主体肿块分界不清,疑肿瘤直接浸润;左侧肩前淋巴结及腮腺亦显著肿大(未示出)。未见骨质破坏或中耳受累。DWI(G)示肿块显著高信号,ADC图(H)对应低信号,提示弥散受限、细胞密度高。T1W:T1加权;T2W:T2加权;DWI:弥散加权;T1CE:增强T1加权;T2:T2加权;ADC:表观弥散系数。
MRI示肿物弥散明显受限(DWI高信号、ADC图低信号),平均ADC值397×10⁻⁶ mm²/s,提示细胞密度高。同侧多个淋巴结(下颌、内侧与外侧咽后、肩前)显著增大、均匀强化且弥散受限,疑为转移;右侧内侧咽后淋巴结轻度增大。未见肺转移、骨质破坏、鼓泡、鼻腔或脑实质异常。
综合影像结果,肿瘤已广泛浸润邻近软组织,无法手术切除。
03 治疗
放疗被选为主要治疗手段。基于影像结果并与宠主沟通后,决定采用姑息性放疗,首要目标是缓解临床症状并缩小肿瘤体积。
治疗模拟时,患猫取胸卧位,使用真空垫、热塑面膜及咬合块固定。为提高解剖勾画与靶区精度,采用融合后的CT与MRI数据(图2)。
大体肿瘤体积(GTV)定义为增强的肿块,包括左耳病灶及同侧腮腺、下颌腺、咽后淋巴结和下颌淋巴结。临床靶区(CTV)在GTV基础上外扩3 mm各向同性,以涵盖可能存在的微小病灶区域,如耳道积液、周围水肿脂肪及耳病灶邻近增厚筋膜,同时避免皮肤、体腔及解剖边界等不必要的范围。计划靶区(PTV)则在CTV基础上再外扩2 mm。危及器官(OAR)包括脑、脊髓、耳蜗、视交叉、视神经、眼球、晶状体、泪腺、唾液腺及皮肤均予以勾画。
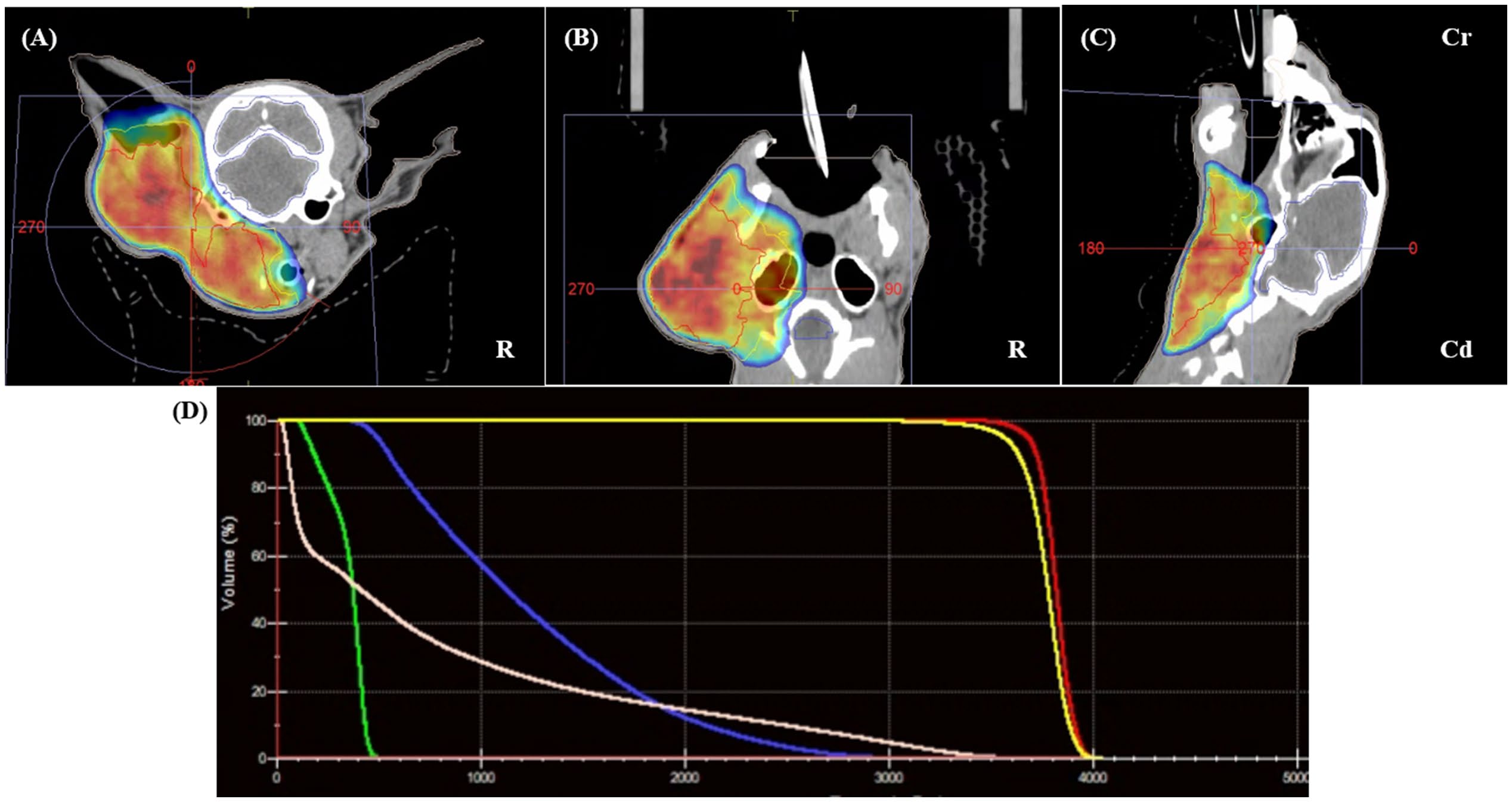
图2. 利用融合的治疗前CT与MRI数据集进行放疗计划。GTV(红色)包括左耳道肿块、腮腺与下颌腺及肿大的同侧淋巴结;未设CTV。PTV(蓝色)由GTV外扩5 mm各向同性生成,涵盖可疑的微小肿瘤延伸区域,同时避开解剖边界。A–C分别显示横断、背侧及矢状平面的靶区勾画;D为剂量-体积直方图,显示处方剂量36 Gy在PTV内的分布,并对OAR施加剂量限制。多模态图像融合及基于蒙特卡罗的VMAT计划实现精准剂量覆盖并保护邻近关键结构。
采用容积旋转调强(VMAT)方案:总量36 Gy,分6次,每周1次,每次6 Gy,疗程6周。治疗计划使用Monaco 6.1.2.0系统,蒙特卡罗算法优化。首要目标:至少98%的PTV接受95%处方剂量;PTV外最大剂量限制在107%。
采用两个共面部分弧,多叶光栅(MLC)准直。患者特异性质量保证(QA)使用VeriSoft v8.1软件及OCTAVIUS 1,500探测器阵列,标准:2 mm/3%剂量差异,通过率≥95%,行动限90%,阈值10%。
治疗时以相同固定装置,使用配备160 μm微多叶光栅的6 MV直线加速器执行;每次治疗前均行锥形束CT验证摆位。放疗按计划顺利完成,无不良事件。
04 预后
放疗初期,鼻周皮肤出现轻度红斑及脓性分泌物,经定期清洁与消毒护理后显著改善,至治疗结束当日(第0天)已基本消退。按兽医放疗肿瘤学组(VRTOG)标准,该反应被评定为1级急性皮肤毒性。未观察到其他与放疗相关的明显不良反应。
第0–180天期间,整体健康状况稳定,未再出现神经症状或耳部瘙痒。肿块体积在随访期内持续显著缩小。
放疗后通过系列影像评估疗效与病情进展:分别于第0天(放疗结束)、第30、90、180天行CT及MRI复查,以监测治疗反应、残留病灶及肿瘤体积、局部侵犯和治疗相关并发症的变化。
第0天,影像显示左外耳道肿块体积显著缩小(图3),但外耳道内仍有残留软组织;此前侵及左腮腺及下颌区域的部分虽已明显回退,仍呈明显强化,边界不清,并推压邻近咬肌向内。同时可见外耳道壁增厚、钙化及少量腔内积液,符合外耳炎表现。左下颌、内侧咽后及肩前淋巴结仍肿大但较前明显缩小;右内侧咽后淋巴结轻度增大。
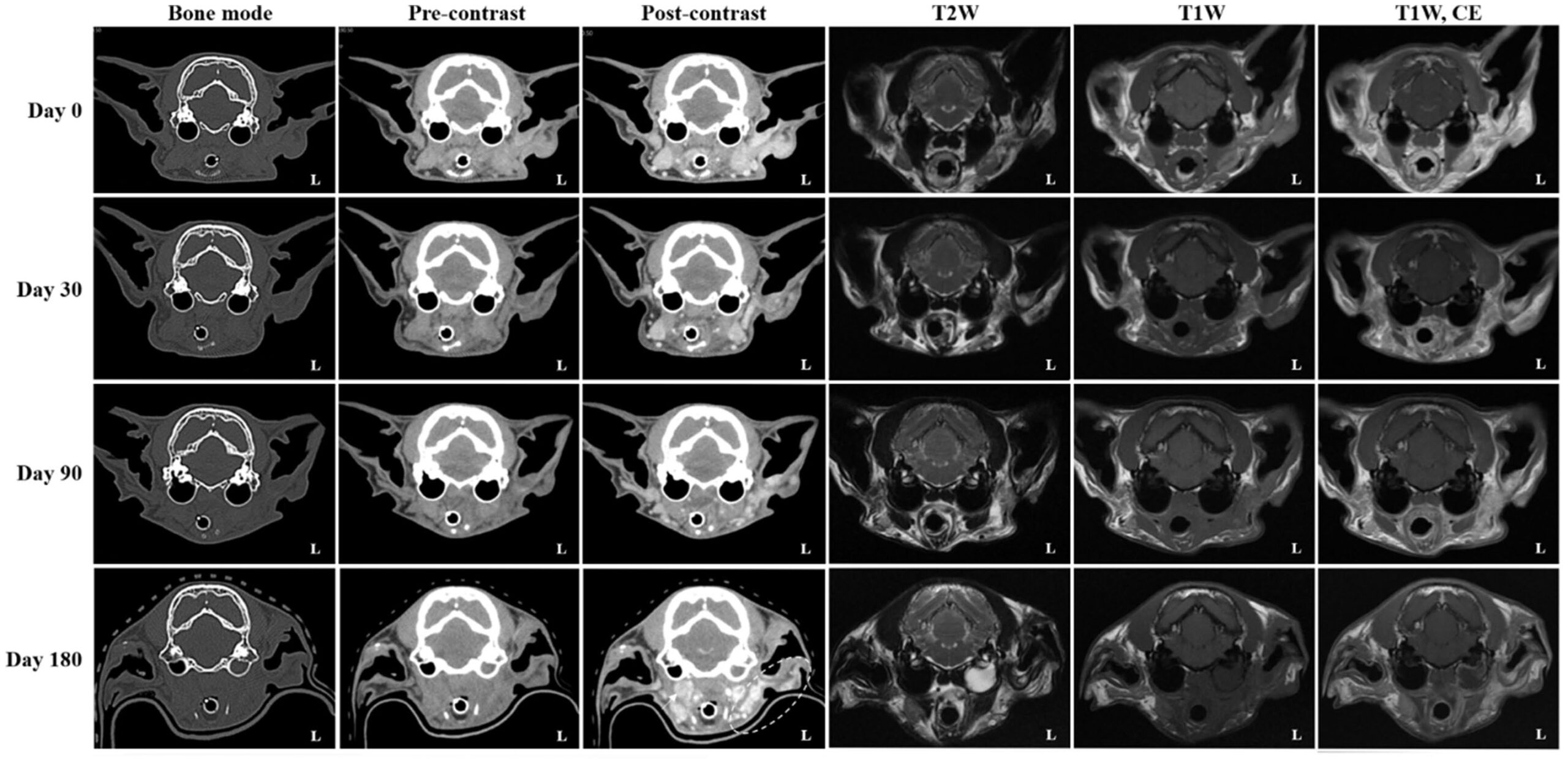
图3. 与治疗前(基线)相比,第0天肿瘤最大径缩小>50%,达部分缓解(PR);第30天再缩小约30%(累计约80%),维持PR;第90天仅再减小约10%,仍处PR;第180天病灶较最低点增大20%,伴区域淋巴结明显增大(箭头,左肩前淋巴结未示),符合疾病进展(PD)。同期CT及MRI见左鼓室积液,符合中耳炎;左腮腺及下颌区(虚线环)强化增加,疑肿瘤进展或复发。
MRI示左下颌及腮腺区DWI高信号、ADC图低信号灶,范围与强度均较治疗前减小(图4)。残留灶平均ADC值469×10⁻⁶ mm²/s,大小9.97×7.69 mm。
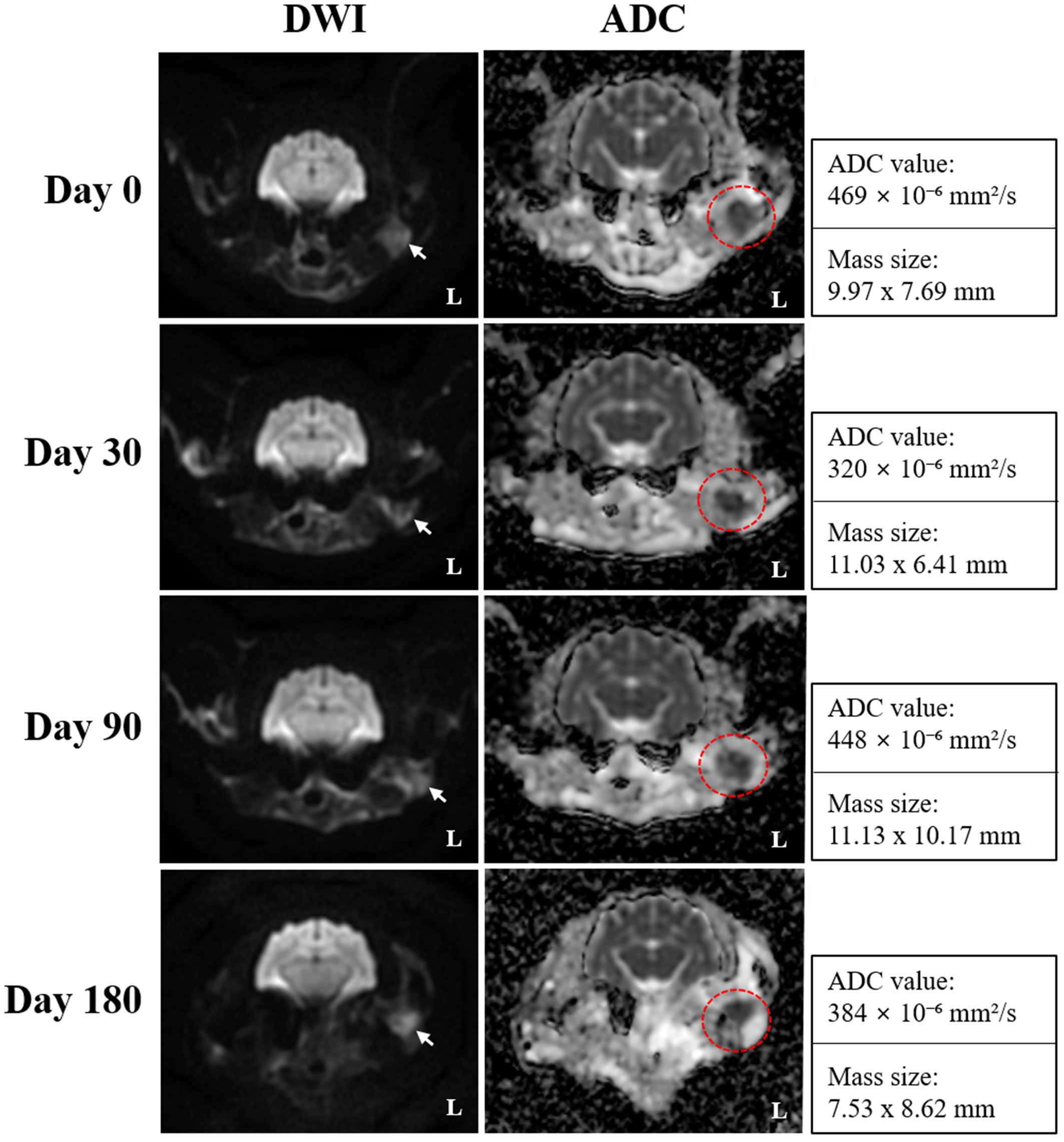
图4. 横断DWI及ADC图像显示局部持续弥散受限,表现为DWI高信号(白箭)及相应ADC图低信号(红点虚线区),在整个随访期间始终可见,提示尽管总体反应良好,仍有肿瘤残余。ADC图可更清晰勾画病灶边界,持续低ADC值反映残留病变内细胞密度仍高。
第30天,CT/MRI示外耳道内肿块进一步缩小。尽管如此,左腮腺及下颌区仍持续可见强化且边界不清;下颌及咽后淋巴结虽继续缩小,仅余轻度增大,但左肩前淋巴结较前次扫描显著增大。DWI/ADC上,高信号灶的大小与信号强度与第0天相仿,平均ADC值320×10⁻⁶ mm²/s,大小11.03×6.41 mm。
第90天,残留灶的大小、范围及影像特征与第30天相比无明显变化;左肩前、下颌及内、外侧咽后淋巴结仍严重肿大,程度类似。DWI高信号灶亦保持稳定,平均ADC值448×10⁻⁶ mm²/s,大小11.13×10.17 mm。左腮腺与下颌区持续异常,提示存在残留肿瘤组织。
第180天,常规CT/MRI虽显示残留灶大小及范围无明显变化,但出现明显疾病进展:左内侧咽后、左肩前及右内侧咽后等多组淋巴结显著增大,左腮腺与下颌区强化程度增加,提示肿瘤可能复发或进展;同时新发左侧中耳炎。平均ADC值384×10⁻⁶ mm²/s,大小7.53×8.62 mm。
依据VCOG v1.0实体瘤疗效评价标准(以病灶最大径为参数):第0天肿瘤较基线缩小>50%,达部分缓解(PR);第30天再缩小约30%(累计约80%),维持PR;第90天仅再减小约10%,仍处PR;第180天病灶较最低点增大20%,伴区域淋巴结显著增大,符合疾病进展(PD)。
05 讨论
耵聍腺腺癌是猫外耳道最常见的原发性恶性肿瘤,起源于改良型顶泌汗腺,局部侵袭性强,可沿软组织间隙浸润至腮腺、颌下腺及咀嚼肌,并早期转移至同侧咽旁、颌下及浅表颈淋巴结。
由于猫耳道解剖狭窄、肿瘤常呈弥漫性生长,临床就诊时多已属晚期,表现为顽固性耳分泌物、甩头、搔耳,若侵犯面神经或前庭结构则出现面瘫、眼球震颤或头斜。
外科“全耳道切除+外侧鼓泡截开术”被视为唯一可能根治的手段,但当肿瘤超越外耳道软骨或侵犯深部腺体时,R0切除几乎不可能,术后复发率>60%。因此,对无法手术的病例,姑息性放疗成为缓解症状、延长生存的核心选择。
既往小规模回顾性研究显示,常规二维放疗中位生存期(MST)仅3-6个月,且急性副作用(外耳炎、角膜炎)发生率高;而容积调强(VMAT)可在保证靶区覆盖的同时显著降低邻近脑干、眼球、唾液腺的受量,为老年猫患者提供了更安全的治疗窗口。
本例14岁波斯猫初诊时即因广泛软组织浸润而失去手术机会,采用VMAT 36 Gy/6次/6周的低分割方案,兼顾生物学等效剂量(BED≈52 Gy₁₀)与耐受性。
治疗前CT显示肿瘤与腺体分界消失,MRI-DWI呈显著高信号,ADC均值仅397×10⁻⁶ mm²/s,提示高细胞密度;同侧多组淋巴结亦出现类似弥散受限,高度怀疑隐匿性转移,临床分期相当于T₄N₁bM₀(VTN类比)。
放疗结束当天,肿瘤最大径缩小>50%,达部分缓解(PR);第30天继续缩小至基线的20%,提示低分割方案对耵聍腺癌具有快速退缩效应。值得注意的是,DWI 上残留灶始终呈局灶性高信号,ADC值波动于320-469×10⁻⁶ mm²/s,虽与传统“有效”后应出现的ADC升高不符,却准确勾画出存活瘤床,提示功能成像在形态学变化不显著时即可识别潜在进展。
第180天,对侧咽后淋巴结突然增大,同侧腮腺/颌下腺强化幅度增加,DWI出现新结节,虽原发灶径线仅增加20%,但综合判断已符合疾病进展(PD)。整个随访期猫体重稳定,未再出现搔耳及神经症状,说明VMAT成功实现了6个月的高质量姑息。
本例亦暴露若干局限:
① 未行穿刺细胞学,无法证实影像判断的淋巴结转移;
② DWI空间分辨率低,对<3 mm病灶可能漏诊;
③ 6个月随访尚不足以评估晚期放射损伤(如鼓泡骨坏死)。
今后可结合超声引导细针穿刺及动态对比增强序列,提高残留/复发诊断准确率;并延长随访至12个月,观察VMAT在耵聍腺癌的真实局部控制持续时间。
总之,猫耵聍腺腺癌侵袭性强,R0 切除机会有限。对无法手术的晚期病例,VMAT低分割姑息放疗可在短期内显著缩小肿瘤、缓解症状,且急性毒性可耐受。CT与MRI-DWI/ADC联合策略不仅能精准勾画靶区,还能在形态学稳定阶段提前发现残留或复发,为后续补量或全身治疗争取时间。
尽管本例最终出现淋巴结转移,但6个月的无症状生存已优于历史报道,提示功能影像引导的精准放疗将成为猫耳肿瘤姑息治疗的重要方向。
文献来源:Kim J, Kim S, Hong S, Kim E, Yoon J, Choi J. Case Report: Palliative radiotherapy monitoring using computed tomography and diffusion-weighted magnetic resonance imaging in a cat with ceruminous gland adenocarcinoma. Front Vet Sci. 2025 Oct 27;12:1682168.