
| 品种:短毛猫 | |
| 年龄:10岁 | |
| 性别:雄 | |
| 诊断:心脏淋巴瘤 | |
01 主诉及病史
因咳嗽两周,疑似慢性心衰而转诊。
既往有控制不佳的糖尿病和猫免疫缺陷病毒(FIV)血清阳性。
02 检查
体重5.3千克。全身乏力,皮肤张力下降。直肠温度36.6°C,心率和呼吸频率分别为190次/分和44次/分。听诊心音低钝、肺部啰音,支气管肺泡音增强。
超声心动图显示心包和胸腔积液、左心房明显增大(左心房与主动脉之比为2.08)、左心室同心性肥厚以及左心室游离壁心肌内的多个斑驳、低回声病变(下图)。
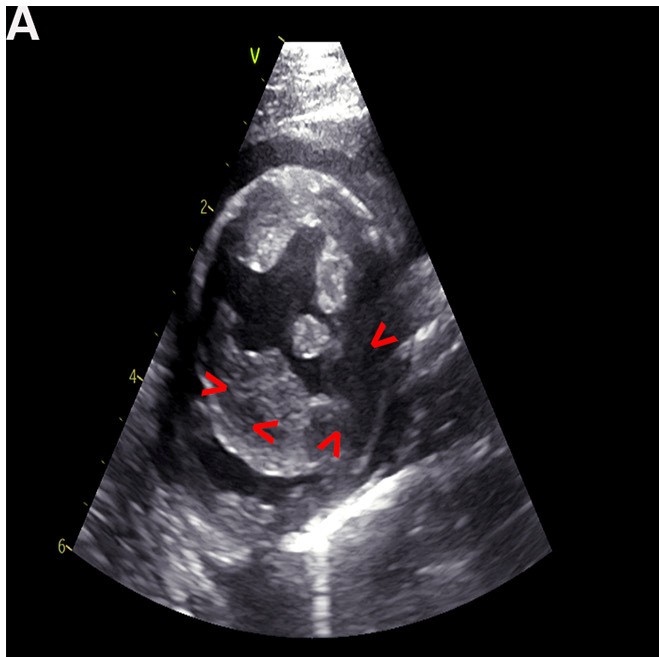
进行了治疗性胸腔穿刺术,获得了积液样本。离心前,液体略显混浊,呈稻草色(总固形物2.0 g/dL;有核细胞总数0.28 K/μL)。离心后显示出混合细胞群,其中有小淋巴细胞(约占40%)和大淋巴细胞(约占30%)。除了少量的反应性间皮细胞外,还观察到中性粒细胞、巨噬细胞和浆细胞(分别约占14%、10%和6%)。很少发现有丝分裂(下图)。
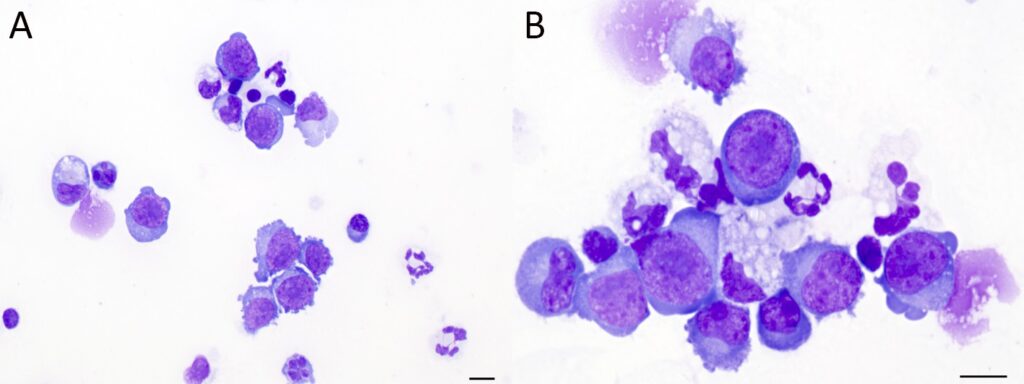
胸腔穿刺术后进行了胸部X光片检查,结果显示心脏肿大、弥漫性斑块状肺泡形态和少量双侧胸腔积液(下图)。
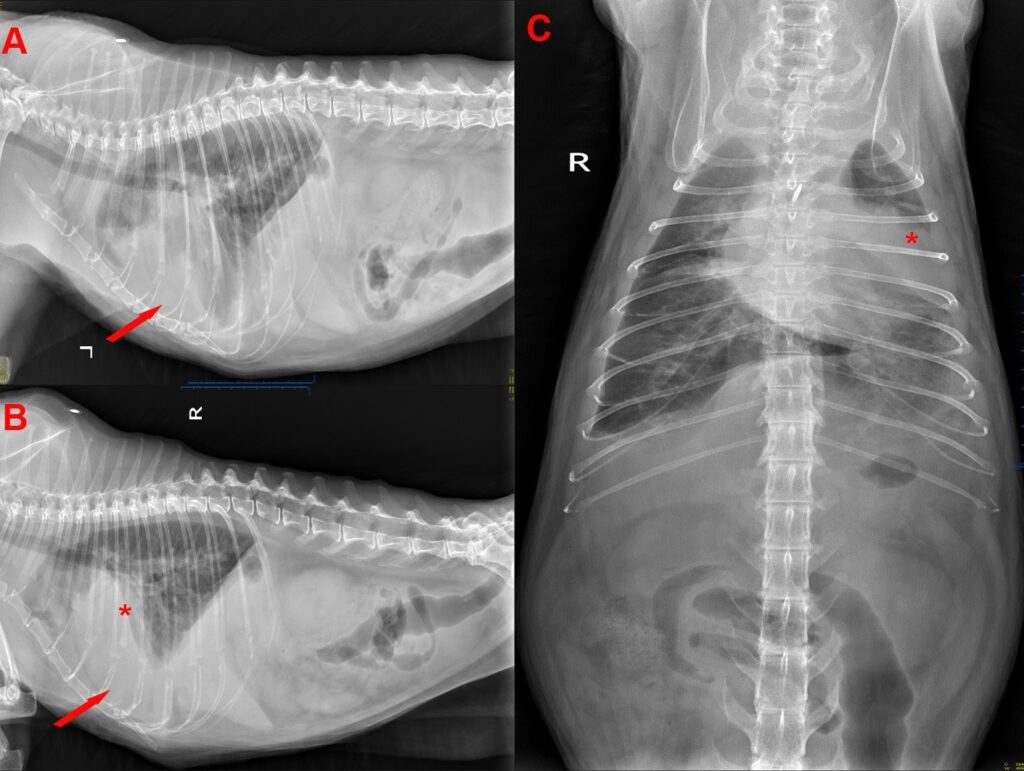
由于担心肿瘤性渗出和预后不良,该患者被实施了安乐死。
03 尸检
胸腔大体检查发现胸膜腔及心包腔含有高蛋白渗出性积液(胸膜腔约35 mL,总固形物2.2 g/dL;心包腔约8.5 mL,总固形物6.8 g/dL)。切片上有多个暗红色、沉重、潮湿的肺实质凝聚灶,渗出血清脓性液体,符合肺水肿(下图)。
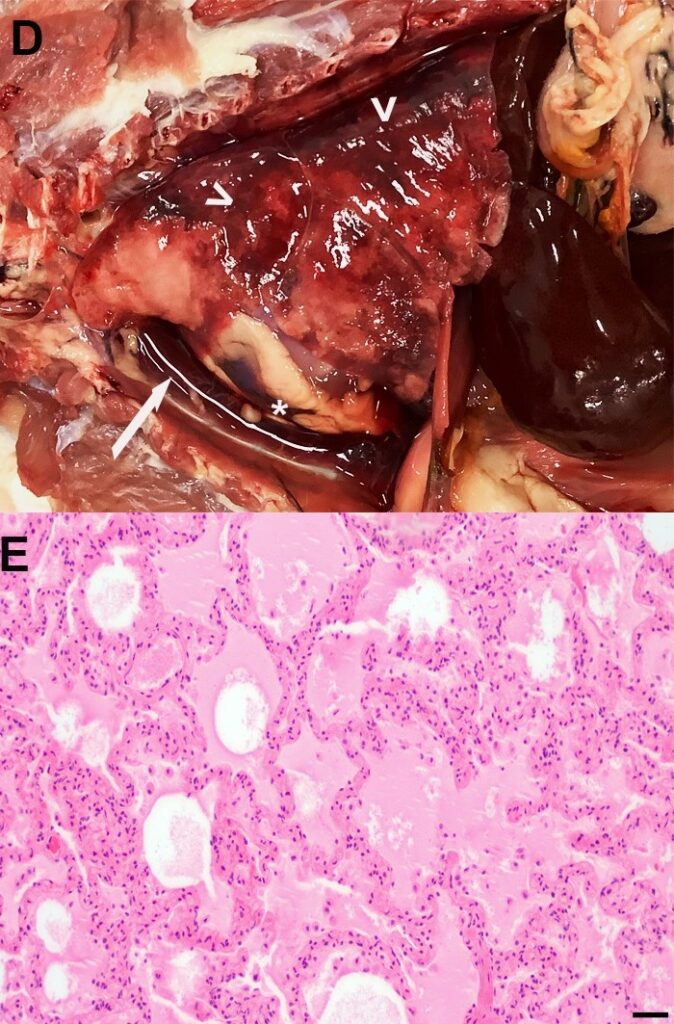
↑ (D)胸部大体检查显示胸膜(白色箭头)和心包(白色星号)积液,发现暗红色和潮湿的肺实质(箭头)凝聚灶。(E)组织学检查证实肺泡间隙中存在均匀的嗜酸性液体(肺水肿)。
切开心包后,观察到多个淡褐色、柔软至易碎的结节状病灶浸润心外膜表面。心脏重31.6克(占总重量的0.59%)。切开心尖后,结节表现为右心室游离壁(RVFW)、室间隔(IVS)和左心室游离壁的跨壁浸润(下图)。
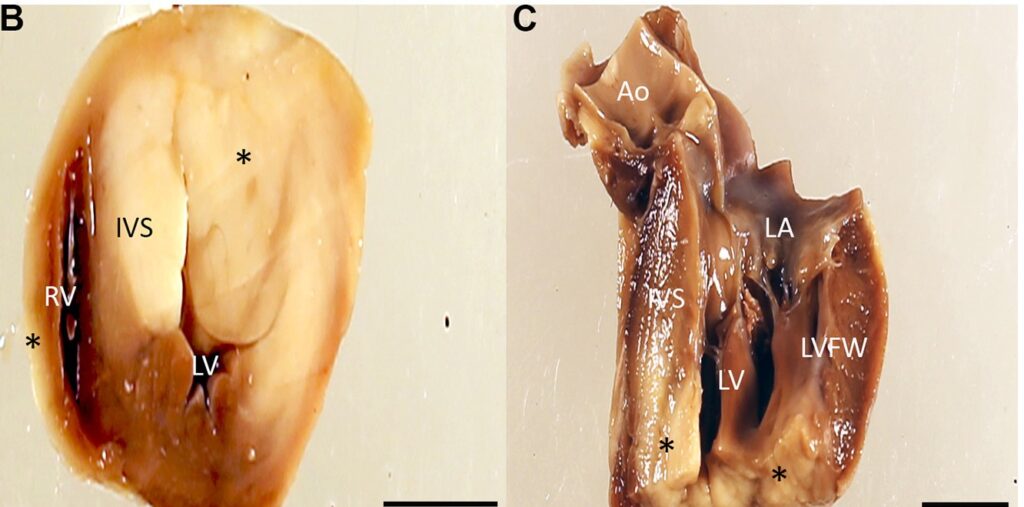
↑ 心脏横向切片距心尖表面约1.5厘米(B),纵向切片穿过左心室流入道(C)。RVFW、IVS和LVFW中浸润有多个横贯壁、界限清楚、无包膜的淡褐色肿瘤性结节病灶(星号)。Ao,主动脉;IVS,室间隔;LA,左心房;LV,左心室;LVFW,左心室游离壁;RV,右心室。
心肌中浸润的中度多形性圆形细胞构成了高度细胞性肿瘤(下图D)。肿瘤细胞的细胞边界清晰,细胞核与细胞质比例较高。肿瘤细胞较大,大多数细胞核的大小约为红细胞的两倍或以上(下图E)。肿瘤细胞核有一到四个突出的核小体,有中度到明显的异形细胞和异形核。每10个高倍视野有12个有丝分裂。浸润的肌纤维广泛坏死,表现出轻度角化、嗜酸性粒细胞增多和碎裂(下图F)。
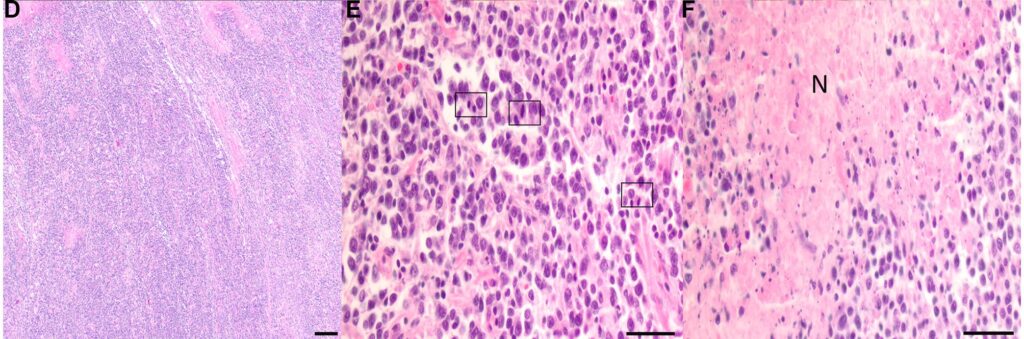
↑ (D)心脏组织的HE染色。宽片状的多形性圆形细胞侵蚀左心室前壁心肌。(E)大块肿瘤性淋巴细胞浸润RVFW心肌,每个高倍视野中有多个有丝分裂图形(方框区域)。(F)在IVS内最明显的是大面积的溶解性坏死(N)灶,其典型特征是嗜酸性细胞增多、肿胀和肌纤维碎裂,并混有大量的核碎屑和少量浸润的小淋巴细胞。
间质纤维物质轻度沉积,Masson三色染色证实存在轻度多灶性间质纤维化(下图)。
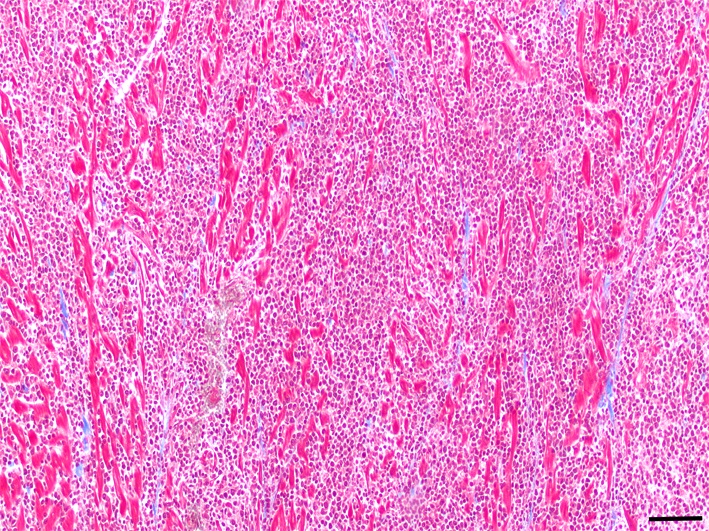
↑ 左心室心肌。间质内多处出现细小的细胞外纤维胶原(蓝色),符合轻度纤维化。
对受影响心脏的切片进行了常规的CD3和CD20免疫组化(下图G)。在肿瘤细胞群中散布着少量至中等数量的小淋巴细胞,这些细胞对CD3有中等程度的膜免疫反应(下图H)。心脏被成片的CD20强阳性大淋巴细胞侵蚀(下图I)。
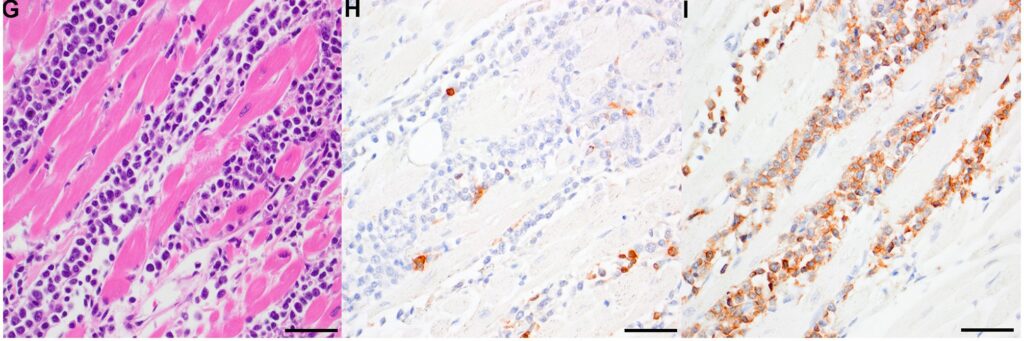
↑ 用HE染色(G)并用CD3(H)和CD20(I)免疫标记的大的多形性淋巴细胞侵蚀RVFW的代表性显微照片。
这些发现支持心脏弥漫性大B细胞淋巴瘤的诊断,该疾病导致的心力衰竭是患者出现临床症状的根本原因。
04 讨论
猫充血性心衰(congestive heart failure,CHF)是小动物急诊和转诊中最常见的临床表现之一,原发性心肌病或继发于全身性疾病(如甲亢、全身性高血压、慢性肾功能不全、肢端肥大症)的左心室重塑通常被认为是前驱病因[1]。
肥厚型心肌病是猫最常见的原发性心肌病,约有15%的家猫表现出临床症状[2,3]。然而,在猫超声心动图检查中发现左心室形态异常时,应考虑心肌肥厚和假性肥厚的其他鉴别因素,包括浸润过程和全身容量耗竭[4]。
超声心动图证实本病例存在左心室肥厚和心包积液,临床初步诊断为左心室同心性肥厚失代偿并伴有房颤。由于糖尿病猫患慢性心衰的相对风险较高[5,6],控制不佳的糖尿病临床病史也被认为是诱因之一。然而,肥厚型心肌病的典型组织学特征(肌纤维肥大/异形、明显的间质纤维化和微血管重塑)并不存在;尸体解剖反而显示出一种跨膜浸润性肿瘤[7]。
心脏肿瘤在猫中很少见,但其中淋巴瘤是最常见的原发性恶性肿瘤[8]。包括淋巴瘤在内的心脏转移瘤更常见于室间隔和左心室游离壁,临床表现取决于心脏内的定位,浸润过程通常会导致心包积液和心力衰竭[9-11]。
该动物在安乐死前几个月的病史中记录有猫免疫缺陷病毒(FIV)血清阳性反应。FIV是一种慢病毒,会导致CD4阳性T细胞逐渐丧失,并引发猫获得性免疫缺陷综合症[12]。与未感染FIV的猫相比,感染FIV的猫更容易患淋巴肿瘤,而淋巴瘤在这些肿瘤中占大多数[12]。
B细胞淋巴瘤在实验性和自然的FIV感染中均有表现,而T细胞和非B/非T细胞淋巴瘤则较少报道[12]。在一组5只动物的病例中,也报道了与FIV介导的心肌炎相关的肥厚性心肌病[13]。
描述猫心脏淋巴瘤的病例报告很少,这是第一例详细描述心脏弥漫大B细胞淋巴瘤(DLBCL)同时伴有FIV血清阳性的报告[9,11,14,15]。本病例的死后诊断显示,DLBCL广泛累及心脏;然而,这究竟是原发性疾病还是转移性疾病,目前仍无定论,因为在肺、空肠、肾、脑、淋巴结(肠系膜和结肠系膜)和骨髓(股骨)中也发现了组织学上类似的肿瘤病灶。
虽然该动物有FIV感染史,但由于实验室缺乏基于组织的FIV检测方法,因此无法对肿瘤组织中的FIV抗原进行进一步评估。不过,历史血清阳性表明淋巴细胞是由病毒介导的恶性转化。
总之,猫左心室肥厚的鉴别诊断应考虑心脏淋巴瘤和心肌炎,对于超声心动图显示心肌肥厚并有FIV病史的病例,建议进行适当的淋巴瘤分子检测。
文献来源:Johnson J, Melhorn H, Karchemskiy S, Karlin E, Bain P, Rush J, Peterson C. Case report: Diffuse large B-cell lymphoma presenting as congestive heart failure in a cat. Front Vet Sci. 2024 Sep 25;11:1467448.
参考文献
1.Kittleson MD, CôtéE. The feline cardiomyopathies: 1. general concepts. J Feline Med Surg. (2021) 23:1009–27.
2.Payne JR, Brodbelt DC, Luis Fuentes V. Cardiomyopathy prevalence in 780 apparently healthy cats in rehoming centres (the CatScan study). J Vet Cardiol. (2015) 17 Suppl 1:S244–257.
3.Kittleson MD, CôtéE. The feline cardiomyopathies: 2. hypertrophic cardiomyopathy. J Feline Med Surg. (2021) 23:1028–51.
4.Sugimoto K, Kawase N, Aoki T, Fujii Y. Effects of dehydration on echocardiographic diastolic parameters in healthy cats. J Vet Sci. (2019) 20:e18.
5.Little CJL, Gettinby G. Heart failure is common in diabetic cats: findings from a retrospective case-controlled study in first-opinion practice. J Small Anim Pract. (2008) 49:17–25.
6.Dobromylskyj MJ, Little CJ. Necropsy findings in a cat with diabetes mellitus and heart failure. JFMS Open Rep. (2021) 7:20551169211055383.
7.Maron BJ, Fox PR. Hypertrophic cardiomyopathy in man and cats. J Vet Cardiol. (2015) 17 Suppl 1:S6–9.
8.Aupperle H, März I, Ellenberger C, Buschatz S, Reischauer A, Schoon HA. Primary and secondary heart tumours in dogs and cats. J Comp Pathol. (2007) 136:18–26.
9.Tanaka S, Suzuki R, Hirata M, Kagawa Y, Koyama H. Unusual diagnosis of feline cardiac lymphoma using cardiac needle biopsy. BMC Vet Res. (2022) 18:251.
10.Woldemeskel M. Primary cardiac lymphoma in a cat. J Comp Pathol. (2020) 174:34–8.
11.Carter TD, Pariaut R, Snook E, Evans DE. Multicentric lymphoma mimicking decompensated hypertrophic cardiomyopathy in a cat. J Vet Intern Med. (2008) 22:1345–7.
12.Magden E, Quackenbush SL, VandeWoude S. FIV associated neoplasms–a mini-review. Vet Immunol Immunopathol. (2011) 143:227–34.
13.Rolim VM, Casagrande RA, Wouters ATB, Driemeier D, Pavarini SP. Myocarditis caused by feline immunodeficiency virus in five cats with hypertrophic cardiomyopathy. J Comp Pathol. (2016) 154:3–8.
14.Amati M, Venco L, Roccabianca P, Santagostino SF, Bertazzolo W. Pericardial lymphoma in seven cats. J Feline Med Surg. (2014) 16:507–12.15.Shih JL, Brenn S, Schrope DP. Cardiac involvement secondary to mediastinal lymphoma in a cat: regression with chemotherapy. J Vet Cardiol. (2014) 16:115–20.