
| 品种:查理士王小猎犬 | |
| 年龄:1岁 | |
| 性别:雄 | |
| 诊断:动脉导管未闭 | |
01 主诉及病史
经胸超声心动图确诊患有亚临床动脉导管未闭(PDA)。
转诊进行微创封堵手术。
02 检查
体重6千克。体格检查显示粘膜呈粉红色、湿润,毛细血管再充盈时间小于2秒,左基底连续性杂音为IV/VI 级,股动脉搏动明显。
经胸超声心动图显示左心房和左心室轻度扩张:左房/主动脉比值1.8 [<1.6],左心室舒张内径1.98 [≤1.7],左心室心尖四腔切面舒张末期容积23.6 mL [≤1.7]。发现了一个小的PDA,最小直径和壶腹部直径分别约为1.2 mm和3.7×7 mm,长度为7 mm(下图)。多普勒超声心动图证实PDA左向右分流,收缩期压力梯度为113.30 mmHg,舒张期压力梯度为59.5 mmHg。
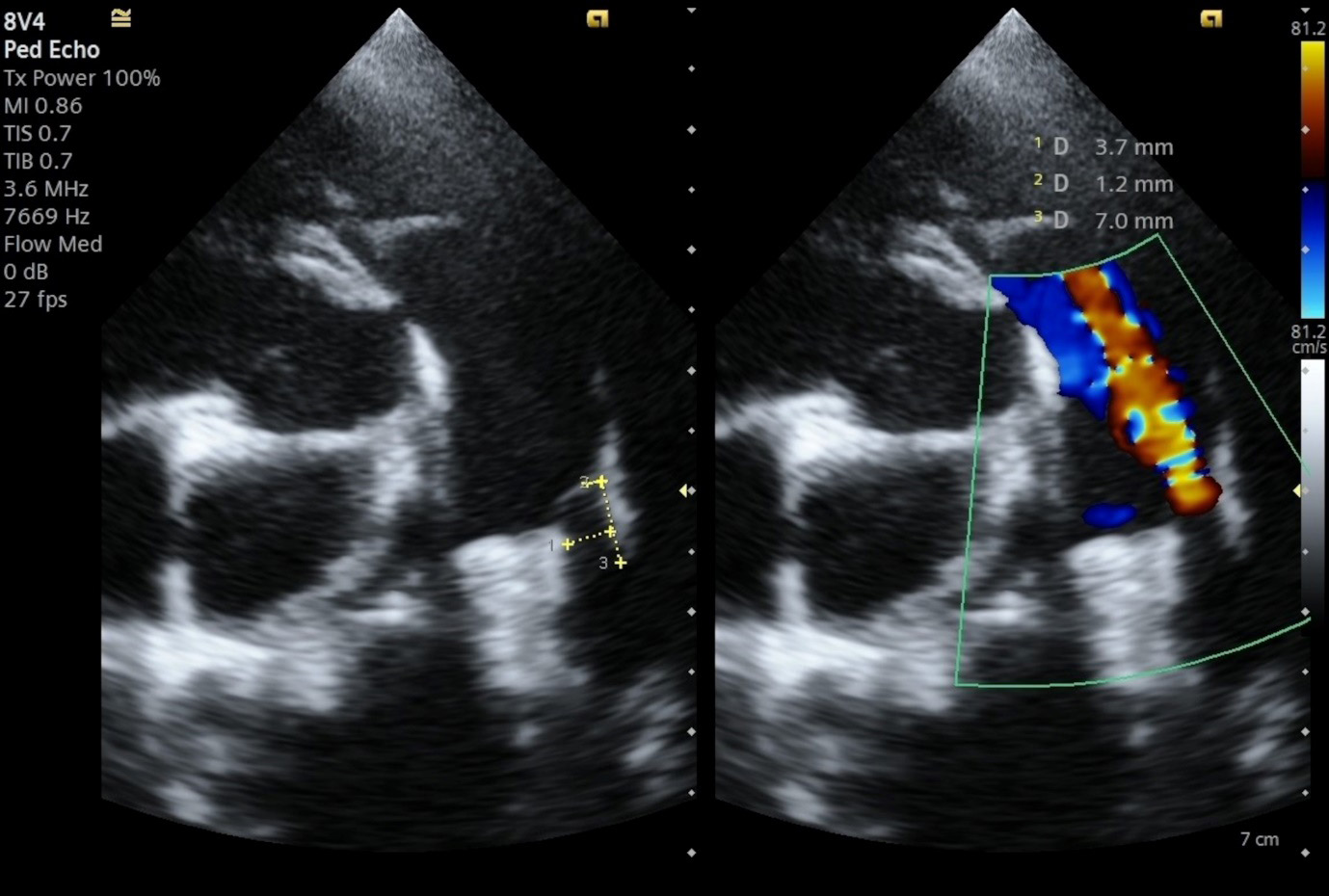
↑ 经胸超声心动图,头颅左侧切面,PDA可视化及其测量(A)和CFM多普勒(双模式)左至右血流。
尽管左心腔负荷过重,但考虑到该犬种的中年患者容易出现二尖瓣关闭不全,从而加重左心腔负荷过重,决定按照主人的意愿,采用微创技术封堵PDA。
03 治疗
该犬的PDA最小直径(1.2毫米)较小,意味着经静脉通道穿越PDA会很困难或耗时,而且即使使用最小尺寸的Amplatzer犬动脉导管闭塞器也会在肺动脉口和壶腹部造成过度拉伸。因此建议通过股动脉入路使用一种新的血管闭塞装置(Micro Plug Set)。
围手术期静脉注射阿莫西林(22 mg/kg)。置于右侧卧位的透视台上,消毒右股动脉区域,为手术做好准备。接受了经食道超声心动图的监测,从而获得了动脉导管的最佳视野及其测量值,证实了对装置的选择(下图)。
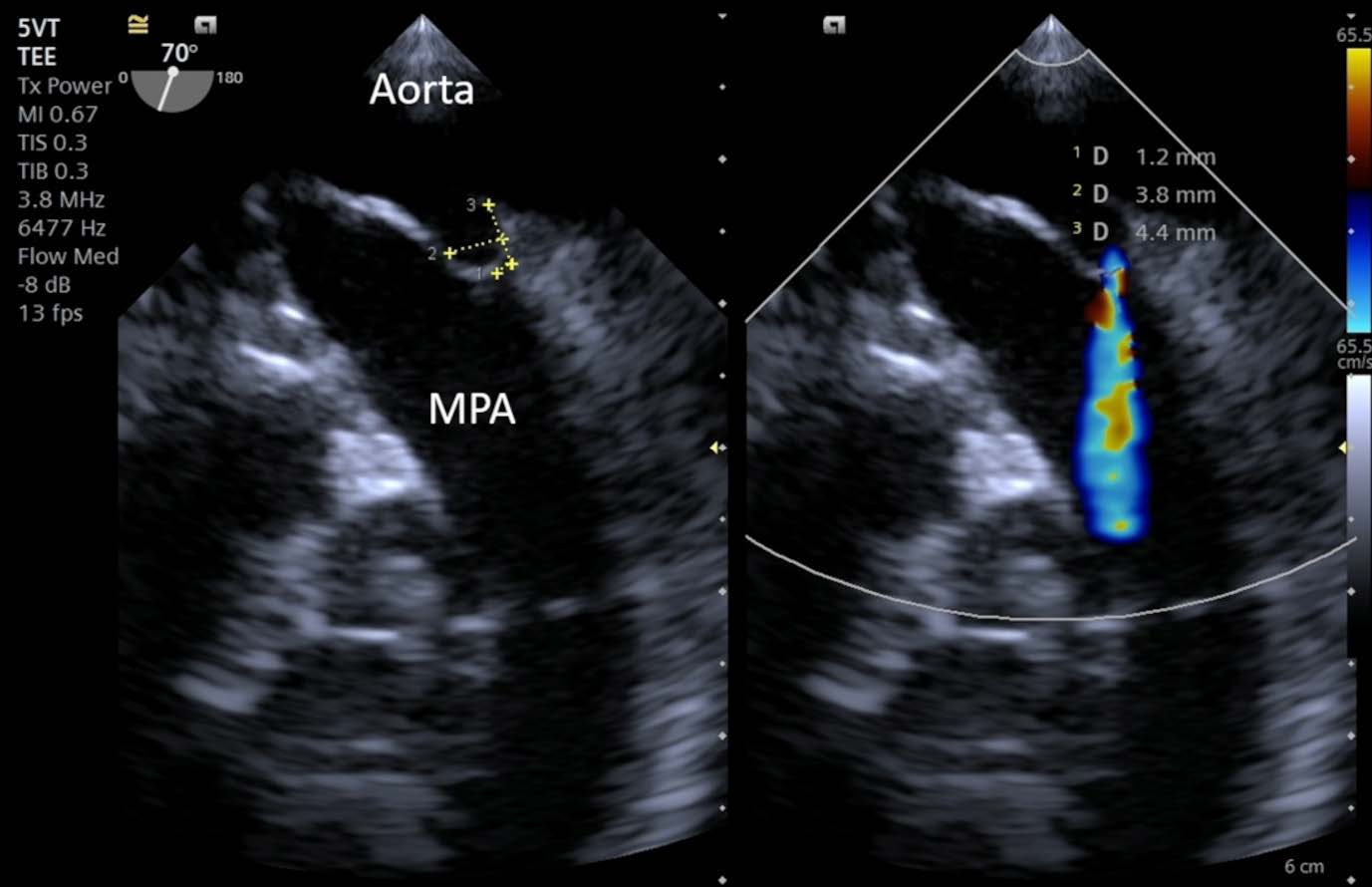
↑ 术中经食道超声心动图显示PDA及其测量值(最小直径1.2毫米;壶腹部直径3.8毫米;长度4.4毫米),以及CFM多普勒(双模式)显示的从主动脉(Aorta)到肺动脉(MPA)的血流。
通过手术切口进入右股动脉,用3-0缝线结扎股动脉远端。用21号针头穿刺动脉后,插入4 French、10厘米长的导引血管鞘,然后插入0.021英寸镍钛诺锥度导丝。
将一根3.3 French的MP血管造影导管连同一根180厘米长的0.025英寸倾斜亲水导丝通过4 French的血管鞘插入股动脉。导丝到达升主动脉后,用3 mL碘化造影剂(350 mg/mL)和3 mL生理盐水稀释后,通过3.3 French的血管导管进行血管造影。血管造影证实了超声心动图先前的测量结果。
随后在透视和经胸超声心动图的引导下,将导丝(重新插入导管)和导管以逆行方式通过PDA进入肺动脉干,直到在肺动脉中清楚地看到导丝的顶端。
然后移除导管,留下导丝,将专用的2.9-French微导管放置在导丝上,使其尖端在透视和超声心动图引导下都清晰可见。导丝随后被移除。考虑到微导管的长度(125厘米),为方便操作并避免与0.0025英寸导丝的长度(180厘米)不匹配,将其顶端缩短了40厘米。
通过制造商提供的Tuohy-Borst Sidearm适配器,将装在装载器中的设备插入输送鞘中,然后小心推进,直到远端圆盘在肺动脉中扩张。轻轻抽出输送导丝和导管,直到肺动脉口出现阻力。然后缩回引导鞘,使装置的中央和近端圆盘在PDA壶腹部内扩张。
随后用推拉“明尼苏达摇摆”手法测试了装置的稳定性,并使用超声心动图验证了经导管血流的停止和装置的正确定位(下图)。然后输送电缆,展开装置。
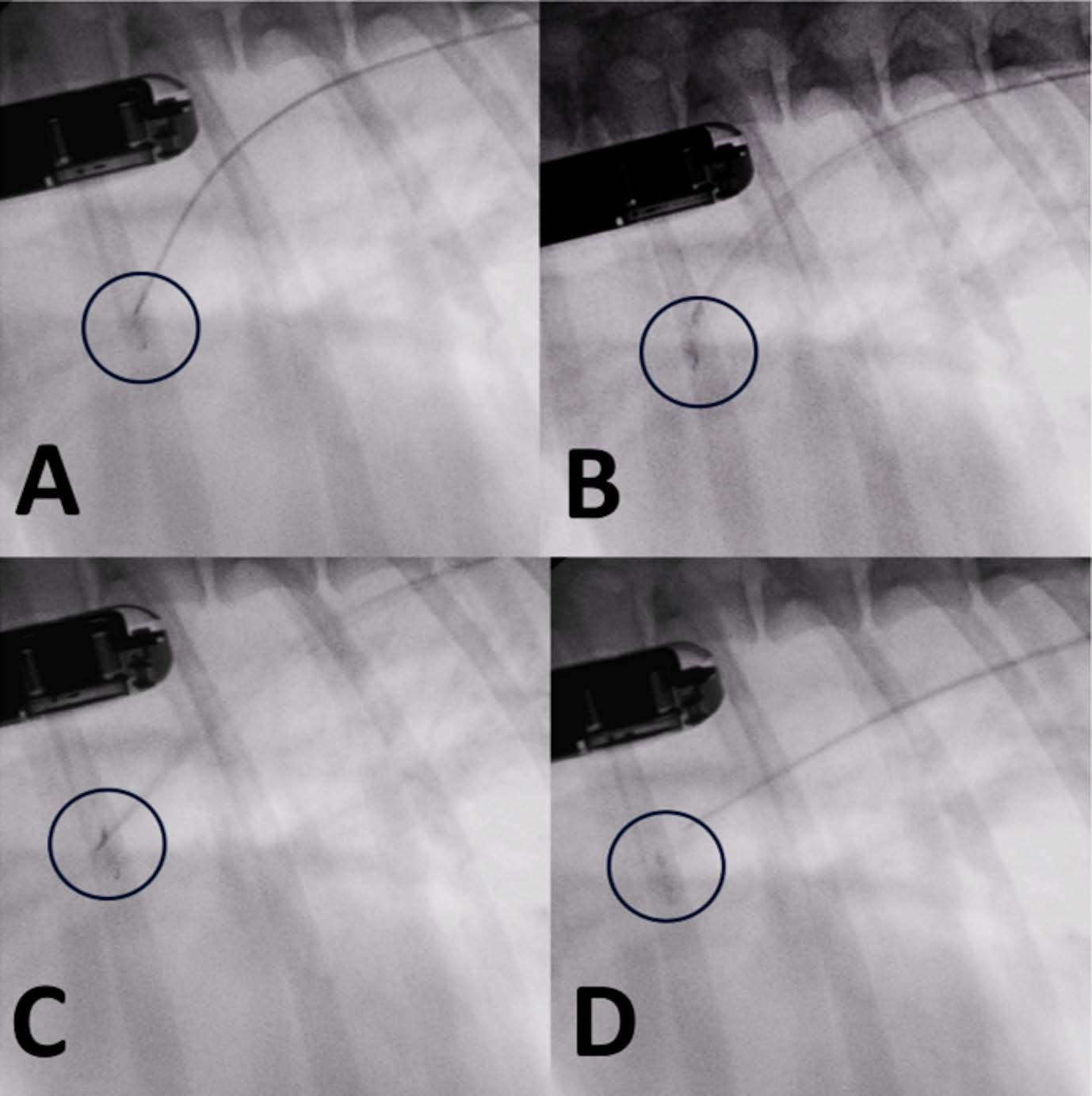
↑ (A)第一个圆盘展开,整个系统回缩,直到与肺门接合。(B)第二和第三个圆盘被释放到壶腹部。(C)逆时针旋转输送电缆,释放装置。(D)移除输送导管和输送电缆。

↑ 术中经食管超声心动图。(A)第一个圆盘被释放到肺动脉中(黄色箭头)。(B)中央和近端圆盘位于壶腹部内(黄色箭头)。(C)CFM(双模式)检查未见残余血流,肺动脉中也未出现血流障碍。
为了进一步验证PDA是否关闭以及主动脉是否有突出物,与之前一样进行了第二次血管造影(下图)。
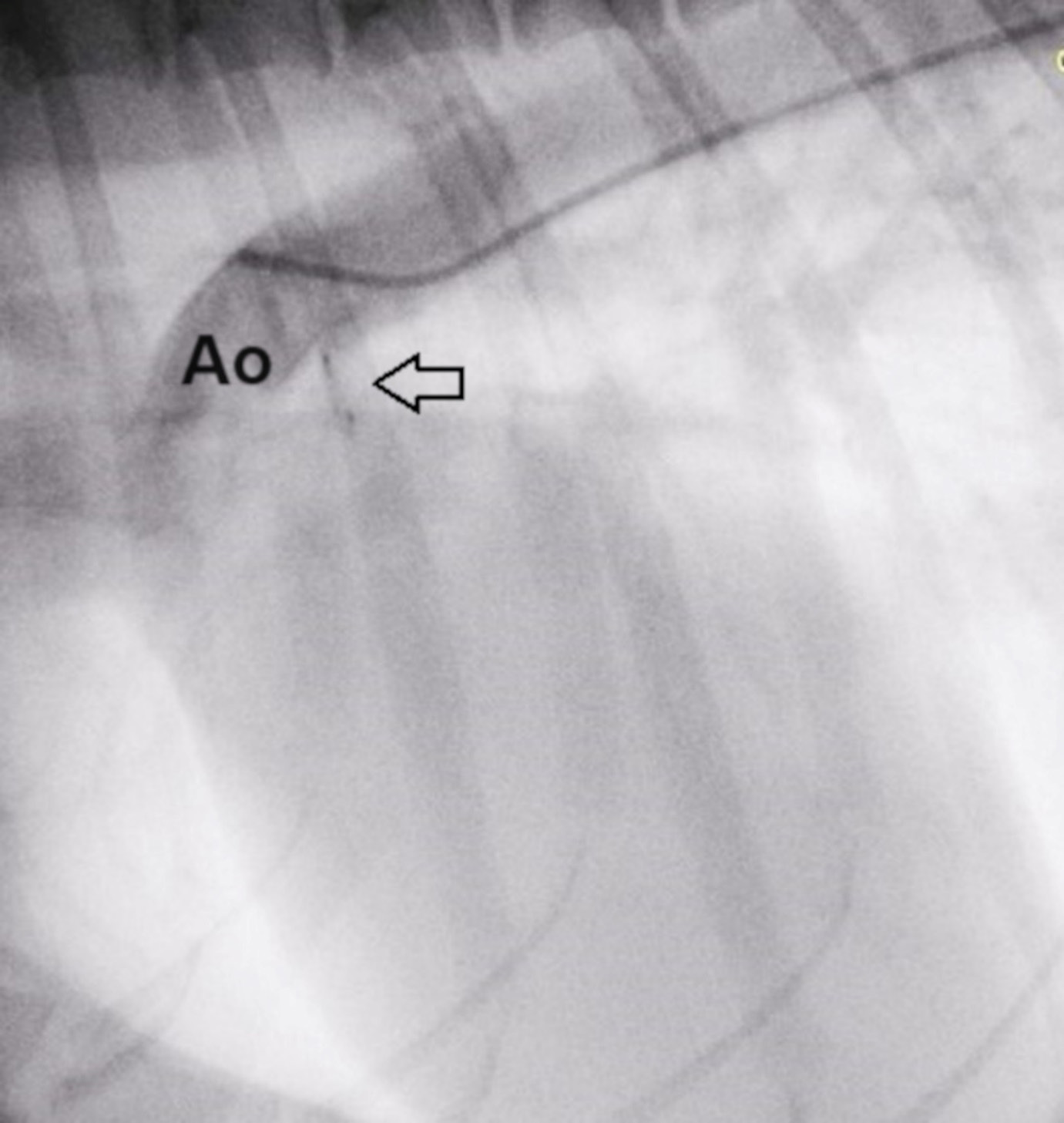
↑ 装置(箭头)释放后进行的血管造影。PDA已完全封闭,看不到残余分流。
然后移除输送鞘和导引鞘,结扎股动脉,并使用3-0缝线以常规方式缝合手术伤口。整个手术持续了40分钟,透视曝光时间为3分40秒。
04 预后
麻醉后恢复顺利,3小时后就能行走和进食。24小时后的胸部X光片显示装置定位正确(下图)。
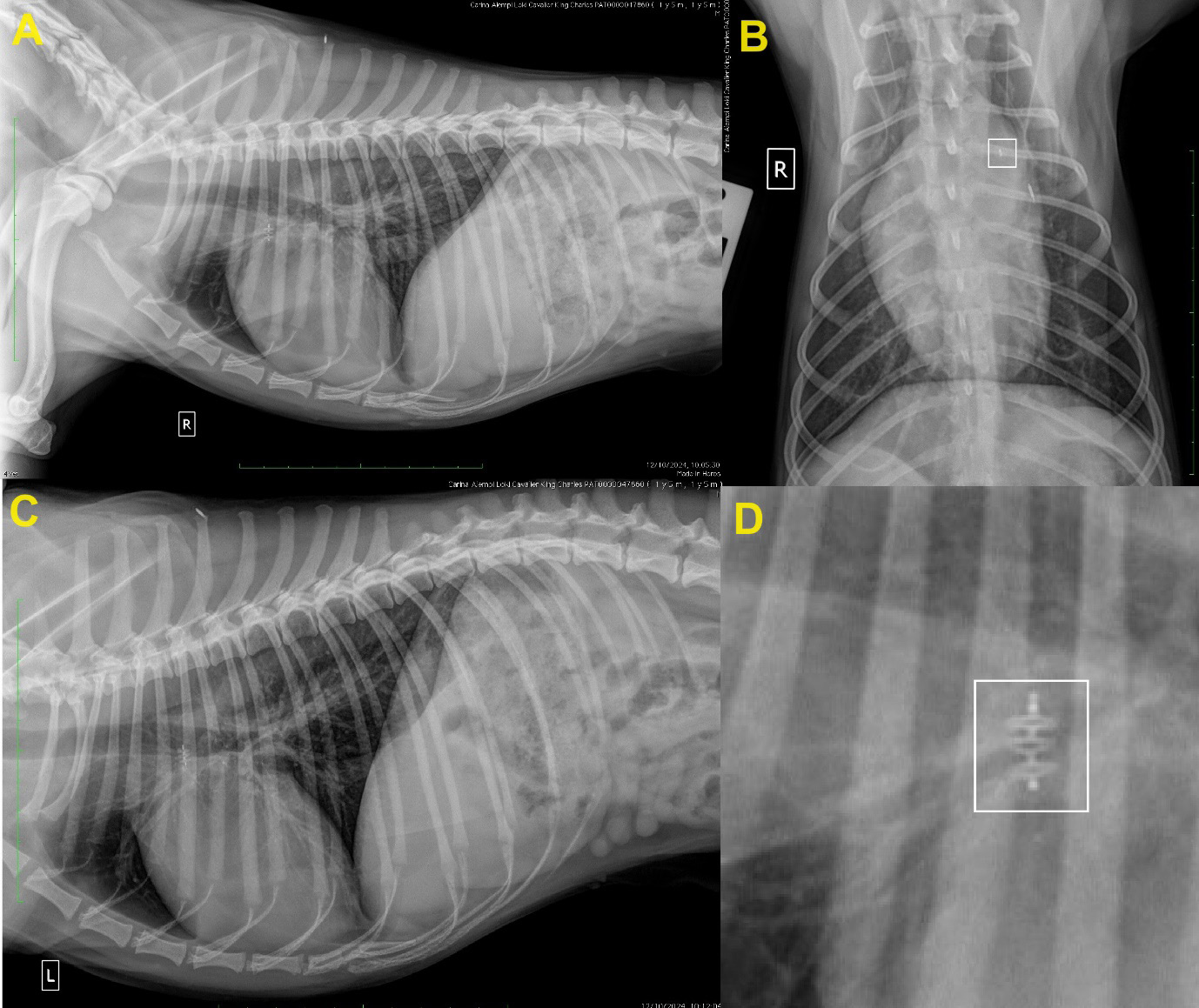
↑ 术后24小时拍摄的胸片。(A)右外侧切面,(B)背腹部切面,(C)左外侧切面,(D)右外侧切面中装置的特写(白色方块)。在(B)中,注意装置(白色方形)的厚度与识别微芯片的厚度相比。术后拍片显示,装置位置正确。
1个月后,超声心动图证实PDA完全闭塞,彩色血流图(CFM)显示无分流,装置定位正确(下图)。
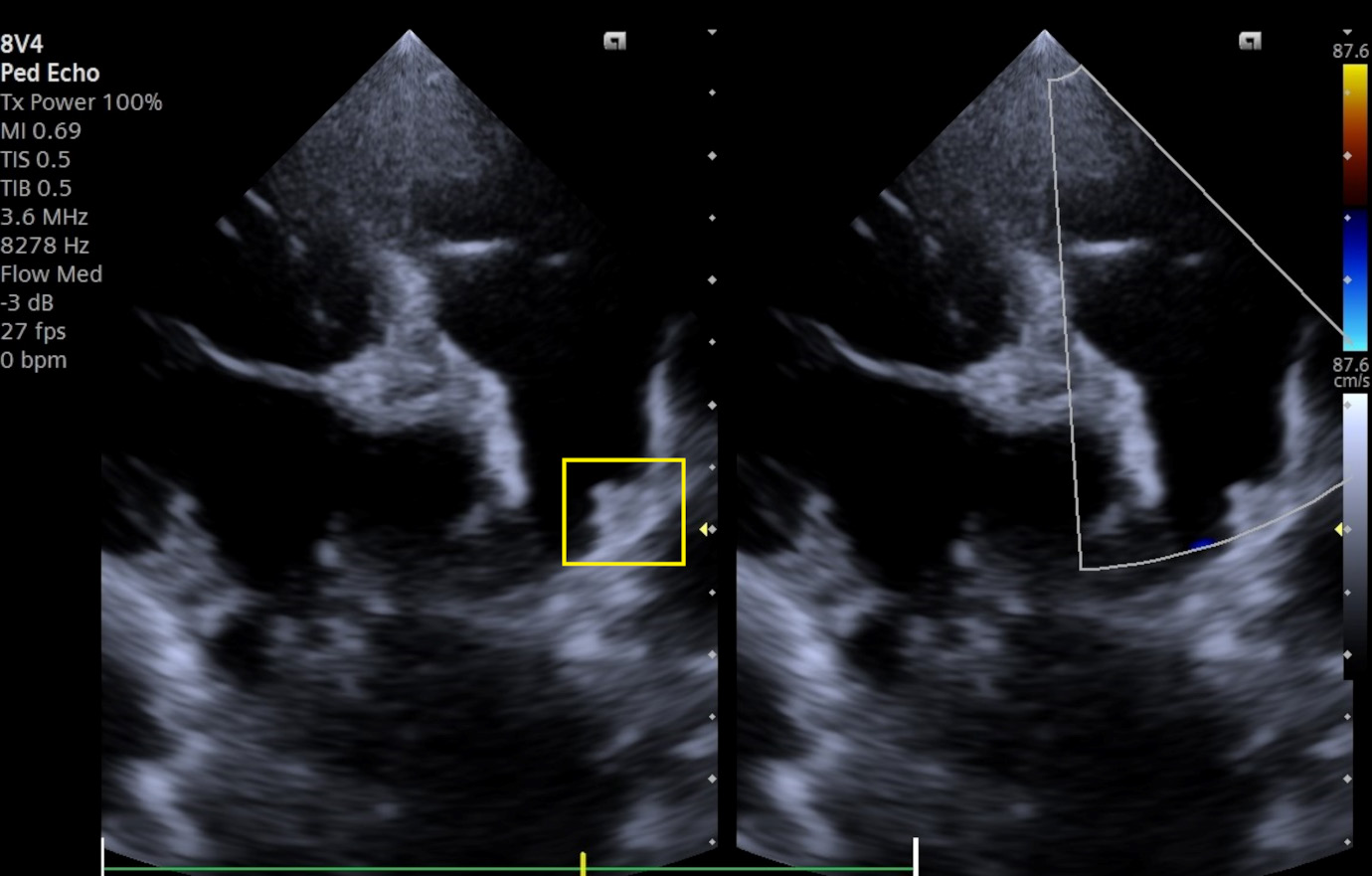
↑ 术后30天的双模式经胸超声心动图。装置(黄色方框)定位正确,CFM多普勒检查未发现残余分流或肺动脉阻塞。
05 讨论
动脉导管未闭(Patent ductus arteriosus,PDA)是犬最常见的先天性心脏病[1]。某些犬种似乎特别容易患上这种疾病,但任何犬种都可能出现这种缺陷,而且雌性犬比雄性犬更常见[2]。PDA左向右分流可导致病理性肺循环过度和左侧容量超负荷,从而可能导致充血性心力衰竭。
多维成像技术描述了多种PDA的大小和形态[3]。在考虑微创经导管封堵时,PDA的形态和大小以及用于血管通路的动脉大小的这种变化会影响封堵建议和设备选择[3]。
专门为患有PDA的犬开发了一种经导管闭合装置:Amplatzer犬动脉导管闭塞器 (ACDO)。目前,心脏病专家将其视为左向右分流PDA犬的首选治疗方法[4,5]。该装置采用微创控制导管输送系统,易于部署,并发症发生率低,而且有多种尺寸可供选择,可用于多种PDA的闭合。
然而,ACDO输送系统的尺寸和通过经动脉途径使用该装置的需要限制了它在小型犬和/或股动脉直径较小的犬中的应用。因此,研究人员研究了外形较小的血管塞,如Amplatzer血管塞4[6,7],这种血管塞也可用于儿童[8]。
Amplatzer血管塞4由两个对称的自膨胀镍钛诺网片组成,有以下尺寸(直径/长度)可供选择:4/10、5/10.5、6/11、7/12.5和8/13.5毫米)。直径的选择有30%-50%的偏差。导管壶腹部的最大直径会增加(限制)其长度,并直接通过4-French的断导管输送,其方法与ACDO植入术类似,无需使用带止血阀的导管[6]。
其他研究人员在使用Amplatzer血管塞2、线圈或其他装置对无法进行常规ACDO封堵的狗进行PDA介入性封堵时,主要采用经静脉方法(股动脉或颈静脉)[9-14]。然而,涉及心腔的经静脉通道可能更具挑战性,逆行进入PDA需要耗费大量时间,有时甚至不可能,尤其是在动脉导管直径较小的病例中。
一种新的血管闭塞装置(Micro Plug Set)已经上市,该装置长度较短(2.5毫米),可通过微导管输送,X光和超声可见。它是为外周血管的动脉栓塞而开发的,早期在几十名新生儿和婴儿中通过经静脉入路进行经导管PDA闭塞手术[15,16]。
Micro Plug Set装置包括一个自膨胀编织的镍钛诺圆柱形网片,网片上有三个大小相等的圆盘,两端各有一条不透射线的标记带(下图)。该装置有四种尺寸,圆盘直径从3-6毫米不等,无约束长度为2.5毫米。据生产商称,该装置使用2.9 French、125厘米长的输送微导管准备和推进,并通过其输送电缆释放。

↑ Micro Plug Set装置示意图,包括装置和2.9 French输液导管,以及相关尺寸(A)和带有毫米刻度的装置照片(B)。
在本研究中注意到的唯一关键问题是该装置的辐射能力较差,而且与其他装置相比,该装置体积较小,透视检查的可见度较低。使用超声心动图进行术中监测除了能缩短操作者和患者的X射线暴露时间外,还能提供有用的支持。对于因探头尺寸而无法进行超声心动图检查的小患者,结合透视进行超声心动图监测可能非常有用,就像用于非常小的早产儿一样[15,17]。
总之,本报告为兽医和人类心脏病专家提供了一种新型的经血管PDA封堵方法,适用于小型犬,也可能适用于儿童,并展示了兽医和人类介入心脏病学领域的相互信息交流如何有助于在解决具有挑战性的临床病例方面取得重大进展。
文献来源:Venco L, Geantă ȘA, Bolintineanu MC, Nechifor A, Leca F. Low-profile KA microplug set for transarterial occlusion of patent ductus arteriosus in a small dog: First experience in interventional cardiology. Open Vet J. 2024 Dec;14(12):3640-3648.
参考文献
[1] Hunt G.B, Church D.B, Malik R, Bellenger C.R. A retrospective analysis of congenital cardiac anomalies (1977–1989) Aust. Vet. Pract. 1995;20:70–75.
[2] Brambilla P.G, Polli M, Pradelli D, Papa M, Rizzi R, Bagardi M, Bussadori C. Epidemiological study of congenital heart diseases in dogs: prevalence, popularity, and volatility throughout twenty years of clinical practice. PLoS One. 2020;15(7):e0230160.
[3] Doocy K.R, Saunders A.B, Gordon S.G, Jeffery N. Comparative, multidimensional imaging of patent ductus arteriosus and a proposed update to the morphology classification system for dogs. J. Vet. Intern. Med. 2018;32(2):648–657.
[4] Nguyenba T.P, Tobias A.H. The Amplatz canine duct occluder: a novel device for patent ductus arteriosus occlusion. J. Vet. Cardiol. 2007;9:109–117.
[5] Gordon S.G, Saunders A.B, Achen S.E, Roland R.M, Drourr L.T, Hariu C, Miller M.W. Transarterial ductal occlusion using the Amplatz Canine Duct Occluder in 40 dogs. J. Vet. Cardiol. 2010;12(2):85–92.
[6] Hogan D.F, Goldfeder G.T. Transarterial correction of patent ductus arteriosus in small dogs with the Amplatz™ vascular plug 4: a pilot study. J. Vet. Cardiol. 2021;35:48–54.
[7] Hulsman A.H, Breur J.M.P.J, Szatmári V. Low profile vascular plug for transarterial occlusion of patent ductus arteriosus in small dogs. J. Vet. Intern. Med. 2021;35(1):98–106.
[8] Mini N, Schneider M.B.E, Schneider K. Transcatheter closure of tubular PDA with amplatzer plug 4 in preterm infants weighing between 900 and 3,400 g: the pros and cons. Front. Cardiovasc. Med. 2023;10:1283992.
[9] Blossom J.E, Bright J.M, Griffiths L.G. Transvenous occlusion of patent ductus arteriosus in 56 consecutive dogs. J. Vet. Cardiol. 2010;12(2):75–84.
[10] Bagardi M, Domenech O, Vezzosi T, Marchesotti F, Bini M, Patata V, Croce M, Valenti V, Venco L. Transjugular patent ductus arteriosus occlusion in seven dogs using the Amplatzer vascular plug II. Vet. Sci. 2022;9(8):431.
[11] Belachsen O, Sargent J, Koffas H, Schneider M, Wagner T. The use of Amplatzer vascular plug II in 32 consecutive dogs for transvenous occlusion of patent ductus arteriosus. J. Vet. Cardiol. 2022;41:88–98.
[12] Hildebrandt N, Stosic A, Henrich E, Wiedemann N, Wurtinger G, Schneider M. Transvenous embolization of moderate to large patent ductus arteriosus in dogs using the Amplatzer vascular plug II. J. Vet. Intern. Med. 2022;36(1):20–28.
[13] Morgan K.R.S, Stauthammer C.D, Barncord K, Pinkos A, Fundingsland S, Rishniw M. Transvenous detachable coiling of patent ductus arteriosus in small dogs. J. Vet. Cardiol. 2022;42:65–73.
[14] Cala A, Ferasin L, Ferasin H, Domenech O, Bini M, Valenti V, Venco L. Transvenous closure of patent ductus arteriosus with Nit-Occlud® PDA occlusion system in 13 dogs weighing less than 3 kg. J. Vet. Cardiol. 2024;56:23–34.
[15] Heyden C.M, El-Said H.G, Moore J.W, Guyon P.W, Katheria A.C, Jr, Ratnayaka K. Early experience with the Micro Plug Set for preterm patent ductus arteriosus closure. Catheter Cardiovasc. Interv. 2020;96(7):1439–1444.
[16] Guyon P, Duster N, Katheria A, Heyden C, Griffin D, Steinbergs R, Moreno Rojas A, Ratnayaka K, El-Said H.G. Institutional trend in device selection for transcatheter PDA closure in premature infants. Pediatr. Cardiol. 2022;43(8):1716–1722.
[17] Catalán A.I, Condori K, Medina M, Lucena S, Montoya D, Gálvez-Arévalo R. Use of echocardiography in percutaneous closure of patent ductus arteriosus at the Instituto Nacional de Salud del Niño, San Borja, Lima – Peru. Arch. Peru. Cardiol. Cir. Cardiovasc. 2024;5(2):e350.